Objetivos principales
1.
Control metabólico
2.
Mejorar
circulación
3.
Control de
infección
4.
Favorecer cicatrización
Partiendo
del principio de que en el origen del pie diabético participan la infección, la
neuropatía, la vasculopatía y hasta la retinopatía, se puede visualizar fácilmente la importancia del
control metabólico en su prevención. La hiperglucemia crónica, ya sea por sí misma
o en combinación con la hiperinsulinemia y la dislipidemia
características del diabético, se relaciona
con el desarrollo de cada uno de estos componentes patogénicos. Una vez
establecido el pie diabético, la importancia del control metabólico es
determinante para evitar la progresión
de las lesiones y las complicaciones
sistémicas.
Criterios de control
La
importancia que se otorga a las cifras de glucosa en sangre como objetivo
fundamental del tratamiento de la DM depende de que haya una correlación entre
ellas y el desarrollo de complicaciones y secuelas. Puesto que el pie diabético
se relaciona más con la diabetes no
dependiente de insulina, describiremos las medidas para el control metabólico
en esta variedad de la enfermedad.
Son
varios los estudios que avalan el uso del tratamiento intensivo con insulina
para un estricto control glucémico y así prevenir o demorar el desarrollo de
las complicaciones, o simplemente, para garantizar una evolución satisfactoria
en situaciones agudas y complejas, como sucede en el pie diabético.
Las
publicaciones de los estudios del Diabetes Control and Complications Trial
(DCCT), y del estudio Epidemiology of Diabetes Interventions and
Complications (EDIC), junto a muchas más, reafirman lo planteado. 32-37 No
se puede olvidar que a la insulina además de su efecto hipoglucemiante, se le
adjudican acciones inmunomodulador y como factor de crecimiento. La terapéutica
intensiva con dosis múltiples de insulina debe comenzarse desde el principio de
la enfermedad (grado I de Wagner), ya sea con insulina regular convencional o
con análogos de acción rápida, antes del desayuno, almuerzo y cena e insulina
NPH o análogo antes de acostarse. Este esquema de tratamiento con dosis
múltiples es válido para cualquiera de los tipos de diabetes mellitus.
Para evaluar el control metabólico será
necesaria la realización de glucemias en ayunas, 2 horas después de la
ingestión de alimentos y antes de acostarse. Se considerará un buen control
metabólico cuando las glucemias en ayunas oscilen entre 100 a 130 y las posprandiales de 2 horas, entre 140 y
160. Hb glicosilada debajo de 7.
Poder realizar determinaciones de hemoglobina
glucosilada (menor de 6,5 % avalará un buen control durante un período de 5 a 7
semanas),34 junto a determinaciones de fructosamina (que reflejan promedios de
glucemia de 2 a 3 semanas) y glucemias en ayunas y posprandiales (que brindan
información de minutos) sería lo óptimo para el manejo del control metabólico
en el paciente diabético.40 Consideramos que los medicamentos reguladores de la
glucemia orales no son recomendables durante el tratamiento de esta entidad,
pues no aseguran el mejor control glucémico en los pacientes.
alimentación y ejercicio
Las
bases del tratamiento son la alimentación y el ejercicio que por su puesto está
limitada en el paciente con pie diabético, y los medicamentos orales, sin
embargo, con frecuencia el paciente con pie diabético (PD) requiere el empleo,
aun cuando sea de manera transitoria de
insulina.
La
alimentación es un elemento fundamental en
el tratamiento de la DM, al grado que
en muchos pacientes basta una alimentación
adecuada para lograr el control metabólico. habría que señalar que la
alimentación del diabético ( dieta para
el diabético) no consiste en una reducción de hidratos de carbono o azúcar,
sino, en una perfectamente balanceada,
en una alimentación normal en el sentido de ideal. Si todas las personas,
diabéticas o no se sujetara a una dieta para diabéticos seguramente habría muchos menos problemas de salud, pero mientras que en los no diabéticos
las desviaciones tienen relativamente poca trascendencia, en el diabético la
trascendencia es acentuada. La tendencia de la alimentación debe ser proporcionar energía y los nutrimentos adecuados para mantener un
peso adecuado y, por lo tanto, debe individualizarse, como cualquier otro
tratamiento.
En
términos generales para los adultos el
componente energético de la dieta se calcula de acuerdo con el peso ideal,
entre 20 y 30 Kcal por Kg de peso ideal. El rango tan alto se debe a que las necesidades metabólicas pueden ser
diferentes, en particular en proporción con la actividad física que realice el
paciente, de modo que en un sedentario s e calcularía sobre 20 Kcal y en el activo pueden considerarse hasta 30 Kcal.
La
dieta debe tener entre 55 y 60% de las calorías en forma de Carbohidratos
complejos, 10 a 20 % de las calorías en forma de proteínas y el resto en forma
de grasa. Es conveniente que tenga una buena cantidad de fibra, por lo
menos 35 gr al día.
Tratamiento del
componente isquémico
Mediante la aplicación de las
medidas indicadas y la descarga postural, se consigue la cicatrización total en
el 90% de los casos en la úlcera neuropática no complicada del enfermo
diabético. No obstante, en la úlcera neuro isquémica o isquémica, es preciso
adoptar, además, medidas de tipo farmacológico o quirúrgico encaminadas a
mejorar la perfusión arterial del pie.
Las diversas opciones de la
terapéutica farmacológica tienen su indicación de forma aislada en los estadios
iniciales de la enfermedad, o bien asociadas a la cirugía revascularizadora en
la fase de isquemia crítica.
A pesar de la larga
trayectoria que en la práctica clínica acreditan la mayor parte de los fármacos
actualmente utilizados, no existe suficiente nivel de evidencia clínica sobre
si éstos, de forma aislada o bien asociados al ejercicio físico, aportan una
regresión en la sintomatología de la CI. Entre otras razones, porque no se
dispone del suficiente volumen de estudios y ensayos clínicos controlados que
comparen el proceso de la enfermedad tratada con el de su evolución natural. La
mayoría de estos estudios evidencian defectos metodológicos importantes que
impiden alcanzar conclusiones válidas y generalizables.
Avala este criterio la
experiencia clínica de que la evolución de la enfermedad es favorable en el
grupo de enfermos motivados a seguir las medidas higiénicas como la suspensión
del tabaco y la práctica habitual de ejercicio.
Tratamiento
farmacológico
Vasodilatadores
Antagonistas del calcio;
inhibidores de la ECA; antagonistas de la serotonina (ketanserina,
naftidrofuril); bloqueantes del simpático; papaverina; blufomedil; nicergolina.
Su indicación se basa en la
hipótesis de que pueden favorecer la apertura de la circulación colateral,
hecho que supone el aporte de flujo sanguíneo a los tejidos isquémicos. No
obstante, y debido a esta misma hipótesis, la acción vasodilatadora se
ejercería también en las zonas no isquémicas, hecho que puede sustraer flujo de
las afectadas, acción que agravaría la situación de isquemia. Su efecto
hipotensor aumentaría las resistencias de la circulación colateral.
Estos dos hechos, en
conjunción con la evidencia de que ningún fármaco tiene capacidad de
incrementar el calibre de una arteria con un grado de esclerosis parietal
avanzado, cuestionan formalmente su eficacia clínica, y por tanto no existen
fundamentos para su prescripción en la isquemia de las extremidades inferiores.
En los enfermos hipertensos
afectos de isquemia crítica, y por las razones expuestas, debería evitarse la
prescripción de fármacos antihipertensivos con efecto β-bloqueante.
Agentes
hemorreológicos
Pentoxifilina, dextrano BPM,
prostaglandina E1, rutósidos, antagonistas del calcio, clofibrato, ácido
ascórbico, papaverina.
Las sustancias hemorreológicas
pueden modificar la fluidez sanguínea por efecto sobre la viscosidad sanguínea,
mediante las siguientes acciones:
·
Mejorando la deformabilidad eritrocitaria.
·
Evitando la formación de “pilas” de monedas.
·
Reduciendo la concentración hemática.
·
Modificando la composición plasmática.
La relación existente entre
una viscosidad anormalmente alta y las diversas alteraciones circulatorias se
ha demostrado en el shock, en la isquemia de las extremidades, en la
insuficiencia coronaria y también en la DM. Esta última se acompaña además de
anomalías reológicas, de hiperviscosidad y de alteración en la deformabilidad
de los hematíes, favoreciendo la interacción de las plaquetas sanguíneas con
las paredes vasculares, indemnes o lesionadas.
La indicación de estos
fármacos para el tratamiento de la isquemia de la extremidad, y en el mismo
sentido que hemos mencionado sobre el grupo de los vasodilatadores, es
controvertida.
De este grupo, la pentoxifilina parece ser la
sustancia que acredita una acción terapéutica más demostrada en el tratamiento
de la CI, tanto por su acción hemorreológica como, en menor medida, por su
efecto antiagregante y potenciador de la fibrinólisis. Mejora la
microcirculación en los miembros isquémicos, y los estudios clínicos que más
estrechamente se ajustan tanto a las directrices europeas como a las de la FDA
han demostrado que después de su administración aumenta significativamente el
perímetro de marcha. A pesar de esta evidencia, aún persisten dudas sobre la
eficacia de este fármaco y sobre su valor terapéutico en amplios grupos de
enfermos, y que fundamentalmente se deben al hecho de que no está
suficientemente establecido si el tratamiento a largo plazo mejora la distancia
caminada más allá de lo que podría conseguirse utilizando únicamente los métodos
no farmacológicos de control de los factores de riesgo.
El estudio escandinavo, que
está considerado como el más riguroso de los que han analizado la
pentoxifilina, excluyó a los enfermos diabéticos amparándose en la premisa de
que la neuropatía podría enmascarar el dolor de la claudicación intermitente,
con lo que impediría la valoración objetiva de la capacidad de marcha.
En los enfermos con isquemia
crítica de las extremidades inferiores, la pentoxifilina también ha aportado
beneficios clínicos significativos en términos de disminución del dolor y
mejoría clínica global.
Los datos disponibles indican
que la administración intravenosa de pentoxifilina puede ser valiosa en el
control de los enfermos con isquemia crítica de los miembros en el intervalo
previo de su preparación para la cirugía revascularizadora.
Otros
tratamientos farmacológicos:
Isquemia: El
objetivo primario en el tratamiento de la úlcera neuro isquémica es aliviar el
dolor, mejorar función y calidad de vida de los pacientes, esto se logra al
incrementar la circulación microvascular.
El cilostazol, un
inhibidor de la fosfodiesterasa, a dosis de 100mg dos veces al día, puede ser
usado si la isquemia está asociada a claudicación intermitente,
proporcionándole al paciente mejoría en la distancia al caminar, siempre y
cuando la localización de la úlcera lo permita (nivel de evidencia A)
El ácido
acetilsalicílico (dosis de 75-162 mg/día) y otros antiagregantes
plaquetarios como el clopidogrel (75 mg/día) son importantes en el tratamiento
a largo plazo en pacientes con enfermedad arterial obstructiva en miembros
inferiores pues reduce el riesgo de eventos aterotrombóticos, mejorando el
curso o la evolución de la isquemia crítica.
Prostaglandinas:
Alprostadil, epoprostenol, iloprost
Estructuralmente, las
prostaglandinas son ácidos grasos que el organismo humano tiene capacidad de
generar en todos sus tejidos y células, a excepción de los hematíes.
Regulan el flujo sanguíneo a
los tejidos específicos aumentando la perfusión de los órganos a través de un
efecto vasodilatador y antiagregante.
Está perfectamente establecido
que la producción de prostaciclina en la pared vascular se encuentra
significativamente disminuida en las enfermedades arteriales oclusivas, debido
a que determinados factores de riesgo, entre los que se encuentra la DM,
provocan una disminución de su síntesis con el consiguiente aumento de los
niveles plasmáticos de tromboxano.
Ésta no constituiría una
circunstancia secundaria de la enfermedad, sino que los estudios realizados
establecen la relativa deficiencia de las prostaglandinas como su base
fisiopatológica fundamental, y abren la hipótesis de que su utilización con
fines terapéuticos pueda mejorar las situaciones de isquemia.
En este sentido, existe
evidencia de que la isquemia induce un aumento de la secreción de PGI2 local, y
que ésta puede estar reducida e incluso abolida en la DM.
Las posibles causas, según
autores como Shaker et al, serían:
·
La peroxidación incrementada de los lípidos con
inhibición de la biosíntesis de prostaciclina.
·
La ausencia de factor estimulador de la
prostaciclina en plasma.
·
La presencia de un factor inhibidor de la
formación de prostaciclina en el suero de los enfermos diabéticos.
En terapéutica clínica se
utilizan análogos estables de las prostaglandinas. Las preparaciones sobre las
que se dispone de mayor experiencia son los análogos de la PGE1, alprostadil y
los de la prostaciclina epoprostenol e iloprost.
La unión de alprostadil con un
oligómero cíclico de la glucosa, la alfa-ciclodextrina, mejora
considerablemente la estabilidad química y la hidrosolubilidad de la
prostaglandina E1.
Su indicación terapéutica
básica se establece en enfermos en situación de isquemia crítica en los que no
existe ninguna posibilidad de proceder a una revascularización quirúrgica, o
frente al fracaso de esta.
Paralelamente, se están
llevando a cabo estudios destinados a establecer su acción sobre la
permeabilidad del by-pass fémoro-poplíteo, en base a su efecto reductor de las
resistencias periféricas, antiagregante plaquetario y a su hipotética
disminución de la hiperplasia intimal. Otro punto de investigación actual es el
de la utilización de la PGE1 en enfermos con insuficiencia renal crónica
terminal, frecuentemente asociada o provocada por la DM. Diversos estudios
concluyen que la perfusión intraarterial o endovenosa de PGE1 consigue una
evidente mejoría en la sintomatología isquémica en los enfermos diabéticos.
Las perspectivas de un futuro
inmediato se concretan, por un lado, en la elaboración de prostaglandinas más
estables y en la consecución de presentaciones galénicas que posibiliten su
administración por vía oral y, por otro, en el mejor conocimiento de su
mecanismo de acción a nivel de la microcirculación, con la finalidad de poder
seleccionar de forma más precisa qué tipo de enfermo y qué tipo o grado de
lesión puede beneficiarse de forma más eficaz de su utilización.
Antiagregantes
plaquetarios
Ácido acetil salicílico,
dipiridamol, sulfinpirazona, triflusal, tienopiridinas, dextrano 40
En la fisiopatología del
proceso de formación y crecimiento de la placa de ateroma, las plaquetas están
implicadas de forma fundamental.
Numerosos autores han descrito
la presencia de una hiperactividad plaquetaria en los enfermos diabéticos,
siendo destacables los siguientes aspectos:
·
Hiperadhesividad a las superficies extrañas y a
la membrana basal de los capilares.
·
Hiperagregabilidad en presencia de agentes
agregantes (ADP, colágeno, ácido araquidónico, adrenalina).
·
Defecto de desagregación.
·
Acortamiento de la vida media plaquetaria y
aceleración de su turn-over.
Esta hiperactividad
plaquetaria conduce al incremento de la síntesis y/o liberación de sustancias
intraplaquetarias implicadas en distintas fases de la hemostasia y de la
trombosis. Algunas de ellas parecen ser particularmente pro-agregantes y
potencialmente aterógenas, como el tromboxano A2, los endoperóxidos, el factor
plaquetario 4, la betatromboglubulina y el factor mitógeno o PDGF.
La progresión de la
aterosclerosis está estrechamente relacionada con episodios subclínicos de
trombosis arterial mediada por plaquetas, y la mayor parte de los factores de
riesgo reconocidos en su progresión como son el tabaco, la hiperlipidemia y la
hiperviscosidad sanguínea tienen diversas acciones sobre la activación
plaquetaria.
La principal acción de los
fármacos antiagregantes plaquetarios es su efecto preventivo sobre la formación
de trombos secundarios a la placa de ateroma, y en este sentido, informes como
el Antiplatelet Trialists´ Collaboration y el US Physicians Health Study han
presentado resultados probados en el sentido de que la terapia antiplaquetaria
mejora de forma significativa la permeabilidad de los procedimientos
quirúrgicos de revascularización. No obstante, no se ha corroborado que su
utilización sistemática modifique el curso evolutivo de la enfermedad
ateromatosa.
Figura 1.
Mecanismos de acción terapéutica de los fármacos hemorreologicos
Figura 2.
Nivel de acción terapéutica de los fármacos antiagregantes plaquetarios
Finalmente, sigue vigente la
necesidad de disponer de fármacos antiplaquetarios con mejores perfiles de
seguridad y una mayor eficacia que la que presentan los disponibles en la
actualidad.
El ácido acetil
salicílico (AAS) basa su acción antiagregante plaquetaria en la
capacidad de bloquear la ciclooxigenasa plaquetaria, mediante un proceso de
acetilación que repercute en la formación de tromboxano A2, mientras que sus
metabolitos tienen poco efecto sobre esta enzima. La ciclooxigenasa es una
enzima que interviene en la conversión del ácido araquidónico a endoperóxidos
cíclicos —prostaglandina G2 y prostaglandina H2 —, y puede ser también
bloqueada por fármacos antiinflamatorios no esteroideos, la indometacina, la
fenilbutazona, el ibuprofeno y el naproxeno.
Los efectos del AAS persisten
a lo largo de toda la vida de las plaquetas, ya que la acetilación de la ciclooxigenasa
es irreversible. La función plaquetaria sólo se restablece cuando se suspende
su administración y entran en circulación nuevas plaquetas.
También actúa sobre la
ciclooxigenasa de la pared de los vasos inhibiendo la producción de
prostaciclina.
El AAS ha demostrado, en
ensayos clínicos controlados, su capacidad de reducir el riesgo de nuevos
eventos cardiovasculares en enfermos con isquemia coronaria.
La dosis más ajustada para la
optimización de su eficacia terapéutica es un tema sobre el que persiste el
debate. Algunos autores argumentan que dosis bajas, inferiores a 250 mg/24 h,
pueden ser tan eficaces en la reducción del riesgo trombótico, como aquellas
que superan esta dosis, con la ventaja adicional en la incidencia de efectos
adversos, especialmente gastrointestinales y hemorrágicos.
El dipiridamol actúa
elevando el nivel de AMP cíclico, acción que se traduce en la disminución de la
adhesión de las plaquetas a la superficie arterial lesionada y en su posterior
agregación.
El nivel de AMP cíclico
plaquetario puede incrementarse mediante la estimulación de la adenilciclasa de
la membrana —acción que produce la prostaciclina—, o bien mediante el bloqueo
de la fosfodiesterasa plaquetaria, que previene la disminución del AMP cíclico.
Se ha sugerido que sería este segundo el mecanismo de acción antiagregante del
dipiridamol.
La FDA lo cataloga como
vasodilatador coronario. No obstante, el mayor interés de este fármaco radica
en su efecto antitrombótico, que se ha relacionado con el aumento del AMP
cíclico plaquetario.
La
sulfinpirazona es un fármaco uricosúrico utilizado en el
tratamiento de la hiperuricemia. Estructuralmente es semejante a la
fenilbutazona, pero difiere de ésta por poseer una actividad
antiinflamatoria mínima.
Inhibe la ciclooxigenasa de las plaquetas en menor grado que el AAS, siendo su
efecto reversible, ya que sólo actúa en el intervalo de tiempo en que la
concentración plasmática del fármaco es eficaz.
El triflusal basa
su efecto antiagregante plaquetario en la acción de bloqueo de la actividad de
la ciclooxigenasa plaquetaria, al inhibir por vía del ácido araquidónico la
formación de endoperóxidos y, en consecuencia, la de tromboxano A2. Su
estructura química —ácido 2-acetiloxi-4(trifluorometil)- benzoico— se encuentra
relacionada con los salicilatos.
No obstante, no es un derivado
del AAS y carece de la actividad antiinflamatoria de éste.
Aumenta los niveles
intraplaquetarios de AMP cíclico por inhibición de la fosfodiesterasa
plaquetaria, sin influir en la producción de prostaciclina en el endotelio
vascular, motivo por el cual su actividad antiagregante podría ser superior a
la del AAS, como lo demuestran los estudios que utilizan como inductores de la
agregación el ADP y la adrenalina.
El HTP, metabolito principal
de triflusal, también es inhibidor de la agregación plaquetaria.
Las
tienopiridinas (clopidogrel) tienen su acción fundamentada en la
interferencia de la activación de las plaquetas inducida por el ADP, y en la
inhibición de la secreción de gránulos-alfa, así como de la adhesión
plaquetaria, acciones que pueden tener una particular importancia durante la
activación plaquetaria inducida por fuerzas de cizallamiento.
Los diferentes mecanismos de
acción de las tienopiridinas y del AAS justifican su utilización clínica simultánea,
con la finalidad de mejorar y ampliar el espectro de actividad antiplaquetaria
y, de hecho, algunos autores la indican en la prevención de la reoclusión por
trombosis de las angioplastias simples o asociadas a un stent.
El estudio C.A.P.R.I.E.,
aleatorizado y triple ciego, realizado sobre cerca de veinte mil pacientes de
trescientos ochenta centros en los cinco continentes y publicado en 1997,
permitió comparar el clopidogrel con el AAS.
El diseño de este estudio se
basó en los hallazgos del Antiplatelet Trialists Collaboration —metaanálisis de
142 ensayos sobre sustancias antiagregantes y que incluyó a más de 73.000
pacientes con diferentes manifestaciones aterosclerosas— que indica que los
fármacos antiplaquetarios reducen el riesgo de infarto cerebral, miocárdico y
la muerte de causa vascular, en alrededor de un 25% y que esta reducción del
riesgo es comparable entre enfermos con distintas manifestaciones clínicas de
aterosclerosis.
En el mismo se compara la
eficacia y seguridad de clopidogrel a dosis de 75 mg/día, con referencia al AAS
a dosis de 325 mg/día, en cuanto a su capacidad de reducción de episodios de
trombosis cerebral, miocárdica o periférica y a la muerte de causa vascular.
Los enfermos fueron seguidos hasta un máximo de tres años (seguimiento medio de
1,9 años).
El clopidogrel mostró mejores
resultados con respecto al AAS en los tres grupos: del 23,8% en la isquemia
crónica de extremidades inferiores; del 7,3% en la isquemia cerebral y del 3,7%
en la coronaria. Rheo-Macrodex (10% Dextrano 40). Su acción como fármaco
antiagregante plaquetario es multifactorial:
- Previene la excesiva
activación y adhesión de las plaquetas en los injertos sintéticos, en la
superficie de los stents y en el endotelio dañado, debido en parte a su acción protectora
electrostática.
- Normaliza los niveles
elevados del factor VIII, del fibrinógeno y de otros componentes que influyen
sobre el estado de hipercoagulabilidad inducido por el estrés quirúrgico.
- Reduce la viscosidad
sanguínea y aumenta la perfusión periférica, sobre todo a nivel de la
microcirculación.
En función del efecto
combinado de estas propiedades, consigue disminuir la trombogenicidad de los
injertos y mejorar el run-off, aspectos ambos relacionados con la oclusión a
corto plazo de las técnicas revascularizadoras.
En los enfermos diabéticos, el
Rheo-Macrodex con glucosa al 5% no debe utilizarse, sustituyéndose por su
preparación salina al 0,9%.
En el tratamiento de la angiopatía diabética
han utilizado los medicamentos flebotrópicos como
el Daflón® (Diosmina/ Hesperidina), el cual mejora el tono venoso y el drenaje
linfático, acelerando el proceso de cicatrización de las úlceras. También es
capaz de disminuir la hiperpermeabilidad capilar mediante la protección de la
microcirculación en procesos inflamatorios. Se recomienda su administración
durante 2-4 meses los cuales mejoraran la evolución de la herida.
Microangiopatia
En pacientes con microangiopatía y úlceras
diabéticas se han llevado a cabo estudios para evaluar la eficacia de un extracto
hidrosoluble de la corteza del pinus marítimo (Pinus pinaster ssp. atlantica).
Los resultados muestran que este compuesto, además de su actividad
antioxidante, estimula la enzima Óxido Nítrico Sintetasa (eNOS) aumentando los
niveles de óxido nítrico (. ON), lo que podría contrarrestar los efectos de
sustancias vasoconstrictoras como la endotelina, epinefrina y norepinefrina.
(diabetes, 2009)
Además, los efectos de protección adicionales
podrían derivarse de las propiedades establecidas del óxido nítrico en la
disminución de la agregación y adhesión plaquetaria, así como en la inhibición
de la oxidación de las lipoproteínas de baja densidad (LDL), todo lo cual
coadyuva en la protección contra la aterogénesis y trombosis. De esta forma
esta droga muestra ser una herramienta prometedora en el manejo, tratamiento y
control de esta complicación. Otro fármaco cuyo uso se ha ganado un sitio
especial como parte del tratamiento de la microangiopatía es la Pentoxifilina.
La misma mejora la deformabilidad de los eritrocitos, disminuye los niveles de
fibrinógeno y disminuye la agregación plaquetaria, lo cual demostró ser de
mucha utilidad en las manifestaciones isquémicas en pacientes diabéticos. Sin embargo,
los beneficios clínicos de esta droga no han sido totalmente definidos.
(diabetes, 2009)
Anticoagulantes
Heparina,
dicumarol
La indicación terapéutica de
los anticoagulantes se realiza básicamente en aquel grupo de enfermos que
presentan, en función de valoraciones clínicas y analíticas, un riesgo trombótico
elevado: episodios reiterados de trombosis arterial aguda, reagudizaciones
severas de isquemia crónica —grados III-IV—, prevención de retrombosis
posterior a la fibrinólisis, y cardiopatía embolígena.
La heparinización sistémica y
en ocasiones asociada a tratamiento hemorreológico —dextrano, prostaglandina,
pentoxifilina— se utiliza en los enfermos hospitalizados con el diagnóstico de
isquemia crítica y en los intervalos de diagnóstico y evaluación pre-operatoria
que preceden a la revascularización quirúrgica.
Históricamente, la sal sódica
de la heparina ha sido la preparación farmacológica más utilizada, si bien en
la actualidad tiende a sustituirse por preparaciones heparínicas fraccionadas
(heparinas de bajo peso molecular).
Si la indicación de
descoagulación persiste a medio plazo o de por vida, debe realizarse mediante
dicumarínicos
Trombolíticos
Uroquinasa, estreptoquinasa,
rTPA
Su indicación fundamental se
sitúa en la fase de isquemia aguda secundaria a trombosis arterial, ya sea
primaria o secundaria a la obliteración de los procesos revascularizadores
—by-pass, PTA.
Su objetivo es provocar la
lisis del trombo, con la intencionalidad de proceder con posterioridad a la
reparación quirúrgica de su causa. Los fármacos más utilizados son la
uroquinasa, la estreptoquinasa y el rPTA. La perfusión per-operatoria de
uroquinasa puede mejorar el funcionalismo inmediato de aquellos procedimientos
revascularizadores con difícil runoff distal, aunque existe escasa experiencia
en esta indicación.
Manejo
de infección
Tratamiento local según el
grado de ulceración (grados de la escala de Wagner).
Grado 0 Como ya se ha
comentado en capítulos precedentes, es un "Pie de riesgo". No existe
lesión y, por tanto, la actitud terapéutica es de índole preventiva.
Grado I La actitud terapéutica
va dirigida a disminuir la presión sobre el área ulcerada. Habitualmente no
suele existir infección.
Grado II La infección suele
estar presente, por lo que es necesario obtener muestras para cultivo y
antibiograma. Debe realizarse desbridamiento, cura tópica y utilizar
antibioticoterapia por vía sistémica. Tanto en el grado I como en el II es
básica la actuación podiátrica.
Grado III Se caracteriza por
la existencia de una infección profunda, con formación de abscesos y, a menudo,
de osteítis. La indicación quirúrgica suele ser necesaria.
Es preceptivo el ingreso
hospitalario y la realización de cultivos y estudio radiográfico del pie. Debe
valorarse el componente isquémico, frecuente a partir del grado III, mediante
estudios hemodinámicos. Se realizará el estudio angiográfico si existe
indicación de proceder a la revascularización.
Durante el ingreso debe
observarse un especial cuidado sobre el pie contralateral, evitando la
aparición de úlceras en el talón secundarias a la posición de decúbito
prolongado.
Grado IV Los enfermos precisan
de hospitalización con carácter urgente y valoración del componente isquémico,
que en esta fase evolutiva suele estar gravemente afectado.
Habitualmente, debe procederse
a cirugía revascularizadora, en función de evitar la amputación, o conseguir
que ésta pueda realizarse a un nivel distal de la extremidad.
Grado V La gangrena extensa
del pie requiere la hospitalización urgente, el control de la glucemia y de la
infección, y la amputación mayor.
Tratamiento
local del pie diabético (más información en manejo de heridas y cicatrización
del Blog del autor)
El
manejo local de la úlcera así como la selección de la técnica de abordaje de la
misma y el proceso de desbridamiento va a depender de varios factores, entre
ellos: la etiología, las características morfológicas y la forma de
presentación clínica de la úlcera. Cuando la infección afecta capas
superficiales, el tratamiento local con limpieza y debridación mecánica es
usualmente suficiente. Sin embargo, la presencia de infección severa requiere desbridamiento
quirúrgico; este último está indicado en abscesos profundos, fascitis
necrotizante, gangrena gaseosa y síndrome compartimental. En ausencia de
isquemia el desbridamiento será extenso con la finalidad de remover la mayor
cantidad de tejido necrótico; en presencia de isquemia, el drenaje de abscesos
y tejido necrótico se debe realizar luego de procedimientos de
revascularización.
Los apósitos
utilizados para desbridamiento médico están diseñados para mantener la herida
limpia y libre de contaminación al tiempo que promueven la cicatrización de la
misma. En presencia de una úlcera o herida abierta con infección asociada se
recomienda mantener un ambiente húmedo para prevenir la pérdida de vitalidad
celular además que facilita la migración celular a través del lecho de la
herida y promueve la angiogénesis y la síntesis de tejido conjuntivo. La
elección del oposito dependerá del grado de humedad e infección concomitante.
Figura 3. apósitos para cuidado de heridas
Larvaterapia: Aunque no tenemos
experiencia en nuestro centro, este método es utilizado en centros
especializados y es eficiente para la remoción del tejido necrótico a través
del efecto beneficioso que sobre el pH del tejido y la remoción de este tienen
las enzimas proteolíticas existentes en las larvas que destruyen bacterias
durante el proceso digestivo y que, además, favorece la granulación del tejido
útil. Sustancias obtenidas de las larvas muestran gran actividad contra
patógenos gram positivos y negativos y más recientemente contra S. aureus
meticilino resistente.
Factores
de Crecimiento: Los factores de crecimiento juegan un papel crítico, regulando
todos los aspectos de la cicatrización de heridas, y en especial, el factor de
crecimiento epidérmico favorece la síntesis de colágeno y la reepitelización de
las heridas. En nuestro país se cuenta con Heberprot-P® (Ampolla de 75ug), un
factor de crecimiento epidérmico recombinante para inyección intra y
perilesional, 3 veces por semana, hasta un máximo de 8 semanas. Está indicado
en úlceras Wagner III y IV, neuropáticas e isquémicas, siempre y cuando el
proceso infeccioso esté controlado. Los efectos benéficos de traducen en
formación de tejido de granulación en grado variable.
Tratamiento
farmacológico del pie diabético
El
desarrollo de un proceso infeccioso sobre un pie con compromiso tanto
neuropático como arterial constituye un elemento fundamental para el desarrollo
del pie diabético, por tanto, el control de cada factor de riesgo es un blanco
terapéutico en el intento de prevenir o retrasar la progresión de la enfermedad
y su resultado final que es la amputación.
En
línea general el tratamiento antibiótico por sí solo no es suficiente para la
erradicación del proceso infeccioso, sino que debe ir acompañado de un desbridamiento
quirúrgico amplio y profundo del tejido desvitalizado.
El
primer aspecto para tomar en cuenta para elegir el antibiótico adecuado es
conocer los aspectos microbiológicos o gérmenes más comúnmente aislados en
úlceras de pacientes diabéticos, ya que la instauración inicial del tratamiento
se hará de forma empírica hasta obtener los resultados de los cultivos de
secreción. Las infecciones superficiales como erisipela y celulitis son
causadas por cocos gram positivos, en especial Streptococo betahemolítico del
grupo A, B, C y G y Stafilococos aureus. En úlceras moderadas a severa, así
como en osteomielitis predomina la infección polimicrobiana incluyendo gérmenes
como bacterias gram positivas anaerobia, aerobias facultativas y bacilos gram
negativos dentro de los que se incluyen Stafilococos coagulasa negativo,
Enterococos sp., enterobacterias como Echierichia coli, Corinebacteria sp.,
Pseudomona aeruginosa, Bacteroides frágilis y Peptostreptococos e incluso
hongos (Candidas pp). Otros dos gérmenes con alta prevalencia en infecciones de
úlceras diabéticas son S. aureus meticilino resistente y enterococo resistente
a vancomicina, lo que en la actualidad agrega mayor complejidad al tratamiento
de esta patología.
La
mayoría de las infecciones leves son monomicrobianas siendo suficiente el uso
de antibióticos con alta biodisponibilidad oral, dentro de los cuales se
incluye: amoxicilina-ácido clavulánico, fluoroquinolonas (levofloxacina,
moxifloxacina), clindamicina, trimetropin-sulfametoxazol y linezolid. La mayor
parte de estas infecciones sólo requiere 1 y 2 semanas de tratamiento,
debiéndose evaluar al paciente cada 48 a 72 horas. Las úlceras moderadas y
severas usualmente son polimicrobianas, requieren hospitalización y la
administración de terapia antibiótica parenteral. En nuestro servicio se
recomiendan las siguientes combinaciones en este orden:
· Fluoroquinolonas +
Metronidazol
· Cefalosporinas de tercera
generación + Metronidazol
· -Piperacilina-Tazobactam o
Carbapenémicos + Linezolid o Vancomicina
· Ertapenem + Linezolid o
Vancomicina
· Tigeciclina +
Fluoroquinolonas o Amikacina
· Cefalosporina
+ clindamicina y levofloxacina
Al
elegir una terapia determinada, debe tomarse en cuenta la función renal del
paciente y el potencial efecto nefrotóxico de estos fármacos. La duración del
tratamiento en infecciones severas oscila entre 3 y 4 semanas y debe ir
acompañado de un adecuado control metabólico.
Otro
aspecto a tener en cuenta es la presencia de osteomielitis pues ello interviene
en la elección del tratamiento farmacológico y quirúrgico, así como, la
duración del mismo. Por tanto es importante tener en consideración aquellos
factores que predisponen al desarrollo de osteomielitis como son: úlceras
extensas, profundas y crónicas, asentamiento de la úlcera sobre prominencias
óseas o exposición ósea en el sitio de la lesión. La cirugía conservadora
asociada a antibioticoterapia es una opción atractiva en el tratamiento de la
osteomielitis debido a que reduce los cambios en la mecánica del pie y minimiza
la duración de la terapia antibiótica. Se recomienda iniciar antibioticoterapia
por vía parenteral al menos durante una semana y luego según la evolución
clínica y los resultados del cultivo evaluar la posibilidad de uso de la vía
oral y tratamiento mínimo por 6 semanas aunque en algunos casos se aconseja por
un período de 3 a 6 meses. Deben emplearse antibióticos que tengan buena disponibilidad
y penetración ósea como las quinolonas, rifampicina y clindamicina.
Como
parte del tratamiento farmacológico del pie diabético debe incluirse la terapia
para la onicomicosis, pues más que un problema cosmético, constituye un factor
de riesgo para complicaciones serias como la amputación de extremidades. Los
imidazoles son los agentes más activos contra los microorganismos que causan la
onicomicosis; el Fluconazol, a dosis de 150 – 300 mg una vez a la semana por 6
a 9 meses ha mostrado eficacia y seguridad. El Itraconazol presenta menos
efectos adversos y con 200 mg al día por 3 meses se ha observado una cura hasta
del 79%, sin embargo, debido al alto costo, se han recomendado pulsos de
tratamiento con igual efectividad; la dosis usada es 200 mg BID por 1 semana de
cada mes por un lapso de 3 meses.
Las infecciones subagudas y
crónicas suelen ser polimicrobianas, pero es difícil precisar, en la mayoría de
los casos, y a partir de la recogida de muestras de las úlceras o fístulas,
cuáles son los gérmenes responsables de la infección.
En este sentido, numerosos
autores están de acuerdo en que existe una mínima correlación entre los
hallazgos microbiológicos objetivados en las muestras recogidas de úlceras
superficiales y los gérmenes responsables de las infecciones profundas.
Existe incluso relativamente
poca coincidencia entre los hallazgos bacteriológicos obtenidos por legrado o
por lavados profundos con respecto a los que posteriormente se obtienen en los
fragmentos de una extremidad amputada por gangrena.
Estas consideraciones previas
no invalidan que deban seguirse unos protocolos en base a los gérmenes que con
más prevalencia son responsables de las infecciones del PD que, como hemos
mencionado, se trata en general de infecciones subagudas y crónicas
polimicrobianas, en las que se objetivan de promedio de 2,7 a 4,7 tipos
diferentes de gérmenes, con predominio de los aerobios sobre los anaerobios, y
siendo excepcional que estos últimos sean responsables exclusivos de la
infección.
Es útil realizar de forma
reiterada análisis bacteriológicos de las zonas accesibles en función de que
pueden en ocasiones objetivarse gérmenes como el Stafilococcus aureus meticilin
resistente, el clostridio, el enterococo, o la Pseudomonas, que no son
sensibles a los antibióticos administrados o que añaden una significación
especial a la infección.
A modo de resumen, en ausencia
de datos clínicos, la interpretación de la microbiología es compleja en estas
infecciones. Un cultivo de un exudado de una úlcera, herida o fístula, raras
veces nos indicará de forma inequívoca si está infectada o no lo está y cuáles
son con precisión absoluta los gérmenes que desempeñan un papel importante en la
infección.
Sin embargo, la presencia de
una concentración importante de Stafilococcus aureus, de estreptococos, de
gérmenes anaerobios y de bacilos gramnegativos tipo enterobacterias y
Pseudomonas debe hacer sospechar de forma fundada la existencia de infección y
todavía más cuando estos gérmenes se encuentran en un magma de pus, proceden de
una cavidad cerrada, de una estructura profunda infectada,
se encuentran en monocultivo o
son aislados de forma reiterada en sucesivas muestras.
El tratamiento de las
infecciones en el PD ha de ser individualizado, dependiendo de variables como
la fase —aguda o crónica— de la infección, la afectación en mayor o menor grado
de las estructuras profundas, y los gérmenes responsables de ello.
Siguiendo el esquema de J. Gómez,
el protocolo terapéutico ha de responder a las siguientes cuestiones:
Se requiere una clara
evidencia clínica de signos de infección, expresada en la inflamación local y
en la presencia de exudado, con independencia de la presencia de fiebre o
afectación sistémica.
Cuando se trata de una fisura
o una herida superficial infiltrativa que no afecte a los tejidos profundos, el
tratamiento consiste en evitar que el enfermo siga ejerciendo presión sobre la
misma zona. Debe indicarse el reposo y la adopción posterior de medidas
ortopédicas o incluso quirúrgicas correctivas.
En estos casos de infección
superficial, el tratamiento tópico mediante antisépticos o antibióticos puede
tener valor preventivo, aunque poco demostrado.
La objetivación únicamente de microorganismos,
en ausencia de una clínica consistente, debe ser considerada como una
colonización y sólo requiere su seguimiento y el control microbiológico
evolutivo sin instaurar de primera intención un tratamiento antimicrobiano.
Cuando la infección es
moderada-grave requiere su ingreso hospitalario. Es recomendable de forma
inicial y siempre con posterioridad al drenaje desbridamiento quirúrgico,
utilizar antimicrobianos por vía parenteral para conseguir elevadas
concentraciones plasmáticas y tisulares, que coadyuven a una rápida remisión.
Una vez lograda ésta, y en función del tipo de microorganismos aislados en el
cultivo, se valorará seguir la pauta antibiótica por vía oral, dado que, con
determinados fármacos, como las quinolonas —ciprofloxacino, ofloxacino— se
consigue igualmente un nivel de actividad mantenida y por períodos prolongados
Deben seleccionarse siempre
antimicrobianos que tengan una adecuada correlación clínico-microbiológica en
las infecciones mixtas, con buena difusión tisular y excelente tolerancia.
No debe usarse en estos casos
aminoglucósidos parenterales debido a su inactivación en focos supurativos como
los abscesos, su mala difusión en territorios poco vascularizados y por su
toxicidad.
Asimismo, la aplicación tópica
de antibióticos es inadecuada, dada su dudosa penetración y difusión en los
tejidos desvitalizados.
Si se trata de una infección
aguda —celulitis o linfangitis—, una cefalosporina de primera generación o una
penicilina isoxazólica pueden ser el tratamiento adecuado si se aísla el
Stafilococcus aureus, el estreptococo y un tercer germen.
El desbridamiento amplio y
precoz de la zona necrosada constituye una medida terapéutica fundamental como
reiteradamente se expone en este Tratado del pie diabético. No tan sólo es imprescindible
para obtener una mejoría clínica a nivel del pie, sino que habitualmente
implica una más factible compensación metabólica y un evidente mejor estado
general en el enfermo.
En los casos de infección
crónica en que predominan los bacilos gram-negativos, los anaerobios y las
enterobacterias, puede estar indicado un antibiótico con acción anti-anaerobia,
como el metro- nidazol, la clindamicina o la cefoxitina, asociado a un segundo
con acción sobre los bacilos gram-negativos, como la amoxicilina-ácido
clavulánico, la ciprofloxacina, la cefalosporina de tercera generación, o el
aztreonam.
La combinación
piperacilina-tazobactam o el imipenem pueden utilizarse en monoterapia. Si se
aísla algún germen como el enterococo, el Stafilococcus aureus, o una pseudomona
no sensible a los antibióticos administrados, debe procederse a las
correcciones adicionales necesarias.
Los protocolos más habituales
en pautas de antibioticoterapia en el PD están sintetizados en la figura 5.
Figura 5.
Protocolos de tratamiento antimicrobiano en el pie diabético infectado
La duración del tratamiento
dependerá de la clínica, del tipo de estructuras afectadas — partes blandas o
huesos— y del período evolutivo. Con criterio general, será de un mínimo de
tres semanas y un máximo de tres meses si persiste algún foco infeccioso no
totalmente erradicado con posterioridad a la cirugía.
Finalmente, la actualización
de la profilaxis antitetánica no parece recomendarse en nuestro medio dada la
poca frecuencia con la que el bacilo tetánico tiene su punto de entrada a
partir del PD.
Dolor
neuropático:
El
dolor neuropático afecta aproximadamente 16% de los pacientes con DM y trae
consigo importantes implicaciones en la calidad de vida del paciente. La
Sociedad Americana de Neurología, la Asociación Americana de Medicina
Neuromuscular y Electro diagnóstico y la Academia Americana de Medicina Física
y Rehabilitación recomiendan la siguiente terapia farmacológica para el
tratamiento del dolor neuropático, con el aval de la Asociación Americana de
Diabetes(33,34): Nivel de evidencia A: Pregabalina
300–600 mg/día. Nivel de evidencia B: Gabapentin: 900–3600 mg/día,
Amitriptilina: 25–100 mg/día, Venlafaxine: 75 – 225 mg/día, Duloxetine: 60 –
120 mg/día, Dextrometorfano: 400 mg/día, Morfina, Tramadol: 210 mg/día,
Capsaicina crema 0,075% QID.
El
ácido alfa lipoico ha mostrado una reducción moderada del dolor neuropático
(20-24% superior a placebo), sin embargo, la Sociedad Americana de Neurología
no recomienda su uso por no haber evidencia suficiente al respecto. Esto fue
parte de los hallazgos del estudio ALADIN III donde no hubo diferencias en los
síntomas neuropáticos al comparar ácido alfa lipoico intravenoso y vía oral
contra placebo. Contrario a esto, en el año 2006 se publicó el estudio SYDNEY
2, un estudio multicéntrico, aleatorizado, doble ciego, placebo-controlado
donde se utilizó ácido alfa lipoico vía oral a distintas dosis en comparación
con placebo; se demostró que el uso de esta terapia a 600 mg una vez al día
mejora síntomas neuropáticos y proporciona una óptima relación
riesgo-beneficio.
En ausencia de alteraciones
estructurales del nervio, la forma conocida más efectiva para prevenir la
aparición de la sintomatología neuropática es el control metabólico de la DM.
En este sentido, debe conseguirse un tratamiento optimizado que mantenga la
hemoglobina glicosilada (HbA1c) en valores plasmáticos inferiores a 7,5%.
El enfermo diabético debe
estar advertido de los efectos tóxicos que el alcohol y determinados productos
químicos tienen sobre el nervio periférico La sintomatología clínica más frecuente,
es el dolor, las disestesias y las parestesias, que inciden especialmente en
situación de reposo nocturno.
Previamente, debe establecerse
el diagnóstico diferencial con otras causas de dolor.
Figura 6.
Evaluación y diagnostico diferencial del dolor en el pie diabético
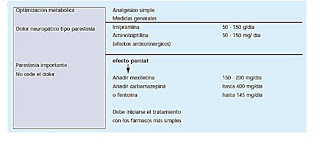
La pauta terapéutica se
efectúa de acuerdo con la escala de dolor descrita por Ross.
Figura 7. Pauta
terapéutica en la polineuritis periférica en el enfermo diabético
El dolor neuropático es un síntoma relevante
en pacientes con diabetes. Hasta 50% de los pacientes diabéticos tiene dolor en
algún momento de su evolución y 15% tiene síntomas agudos.70 El dolor es
constante, molesto y difícil de controlar. Afortunadamente, existen diversos
tipos de medicamentos bien estudiados y que han demostrado efectividad en el
tratamiento, entre ellos los antidepresivos tricíclicos, la carbamazepina,
tramadol, gabapentina, cap-saicina, inhibidores selectivos de la recaptura de
serotonina (ISRS), pregabalina y duloxetina.
Antidepresivos
tricíclicos
Los antidepresivos se han convertido en los
medicamentos de primera línea en el tratamiento de la neuropatía diabética.
Diversas presentaciones y precios los han vuelto medicamentos accesibles y con eficacia
comprobada.
Los antidepresivos tricíclicos, de uso
frecuente en nuestro país (amitriptilina, imipramina), son algunos de los
medicamentos más estudiados, y han demostrado ser efectivos en diversos ensayos
clínicos controlados que involucraron específicamente a pacientes con
neuropatía diabética. Cuando fueron
comparados contra placebo, tanto imipramina68 como amitriptilina
demostraron ser efectivos para disminuir el dolor. Cuando los tricíclicos se
han comparado entre ellos, no ha habido diferencias importantes en su efecto
(NE: I-A).
Algunos estudios clínicos se han enfocado a
interrumpir la trasmisión del dolor con antidepresivos, mismos que inhiben el
recambio de norepinefrina o serotonina. Esta acción central acentúa los efectos
de los neurotransmisores activando sistemas inhibidores endógenos del dolor en
el cerebro que modulan la trasmisión del dolor por la médula espinal. Un
problema pueden ser los efectos adversos, como: xerostomía y disautonomías. La
utilización de nortriptilina en lugar de amitriptilina puede reducir estos
efectos anticolinérgicos.
Tramadol
El tramadol es un analgésico que actúa a nivel
central y se utiliza para tratar dolor moderado o severo, y se ha demostrado
que puede aliviar el dolor en pacientes con dolor neuropático.
Inhibidores
selectivos de la recaptura de serotonina (ISRS)
Estos inhibidores son de uso común como antidepresivos,
pero han sido estudiados como posibilidades terapéuticas para el dolor de la
neuropatía diabética. El citalopram, la
paroxetina y la fluoxetina se compararon con placebo en ensayos clínicos aleatorizados y resultaron
efectivos (NE: I-A).
Antidepresivos
duales
La venlafaxina es un inhibidor de la recaptura
de serotonina y norepinefrina que se ha estudiado recientemente y se considera
efectivo, con la ventaja de que no tiene muchos efectos adversos.
La duloxetina es un potente inhibidor
selectivo con alta afinidad
por los transportadores de recaptura noradrenérgica y serotoninérgica. No parece modular
directamente la función
dopaminérgica y carece de actividad significativa por los receptores histaminérgicos, colinérgicos y
adrenérgicos.
La eficacia y seguridad de
duloxetina en el tratamiento del dolor
de la neuropatía diabética periférica se estudió en un ensayo multicéntrico
doble-ciego en 457 pacientes con dolor debido a polineuropatía por diabetes tipos
1 y 2 durante 12 semanas de tratamiento. Los pacientes se asignaron al azar a
recibir 20, 60 y 120 mg/día, repartidos en dos dosis, o placebo. Tanto con las
dosis de 60 como con 120 mg/día de duloxetina se obtuvo una mejoría significativa comparado con placebo
en la escala “24- h Average Pain
Score”, comenzando esta mejoría una semana después de iniciar el tratamiento y
continuando hasta la semana 12 del mismo. Menos de 20% de los pacientes
abandonaron el tratamiento debido a los efectos adversos. Los autores
concluyeron que duloxetina a dosis de 60 y 120 mg/día resultó segura y efectiva
en el control del dolor neuropático periférico de naturaleza diabética. Se
recomienda como tratamiento de primera línea. (NE: I-A).
Medicamentos
anticonvulsivantes
Diversos medicamentos cuya principal
indicación es el control de crisis epilépticas se han utilizado con éxito en el
tratamiento del dolor neuropático en pacientes diabéticos.
La carbamacepina es uno de los medicamentos
más utilizados con este fin. Múltiples
estudios doble ciego y controlados con
placebo han demostrado que la carbamazepina puede ser útil en el control del
dolor en pacientes con dolor neuropático. Sus efectos tóxicos pueden limitar su
indicación en algunos pacientes (NE: I-A).
La difenilhidantoína se ha utilizado desde
hace tiempo en el tratamiento del dolor causado por neuropatías. Algunos
estudios doble ciego cruzados no han demostrado eficacia en este tipo de pacientes en comparación con grupo placebo.79 Además, sus efectos adversos
disminuyen su uso en pacientes diabéticos, como es el caso de su habilidad para
suprimir la secreción de insulina, misma que ha resultado en precipitación de
estado hiperosmolar y cetoacidosis diabética. (NE: I-A)
La gabapentina es un anticonvulsivo
muy eficaz, pero de mecanismo de
acción no muy claro, pero se han localizado sitios
de unión con alta afinidad en el sistema nervioso central que corresponden a canales de calcio
dependientes de voltaje y que contienen subunidad alfa-2-delta-1. Estos canales
son presinápticos y pueden modular la liberación de neurotransmisores
excitatorios que participan en la nocicepción.
Además, posee un efecto analgésico en la
neuropatía dolorosa. En un estudio multicéntrico efectuado en Estados Unidos,80
la monoterapia con gabapentina fue
eficaz en el control del dolor y en la interferencia
en el sueño asociada con dolor neuropático periférico. También se observaron
efectos positivos en el estilo y calidad de vida. La gabapentina ha sido
estudiada en cuatro ensayos clínicos controlados con placebo, encontrándose que
es un medicamento efectivo y seguro. (NE: I-A)
La pregabalina ha demostrado alivio del dolor
frente a placebo y disminución de la interrupción del sueño por dolor durante
las noches. Se inicia con dosis de 75 mg al día y puede incrementarse hasta 600
mg. Obtiene mejoría rápida (desde la primera semana y se mantiene de manera
evolutiva hasta la quinta semana) y sostenida. Los efectos adversos más
frecuentes son: somnolencia, mareo y náusea (NE: I-B).
Ácido
tióctico
El efecto benéfico antioxidante del
ácido tióctico en los síntomas y
signos neuropáticos se ha demostrado consistentemente, en forma experimental y
en varios ensayos clínicos controlados, sobre todo por sus efectos en el estrés
oxidativo.
En un metaanálisis que incluyó los cuatro
ensayos clínicos controlados más representativos de ácido tióctico en neuropatía diabética (Alpha-lipoic Acid in
Diabetes Neuropathy (ALADIN I, ALADIN III), Symptomatic Diabetic Neuropathy
(SYDNEY) y Neurological Assessment of Thioctic Acid in Neuropathy (NATHAN II))
se comparó al ácido tióctico en dosis de 600 mg al día en infusión intravenosa
durante tres semanas (con descansos los
fines de semana) contra placebo. La
población estudiada incluyó a 1,258 pacientes y se demostró que la tasa de
respuesta favorable fue superior en los pacientes tratados con ácido tióctico
(52.7%) en comparación con los tratados con placebo (36.9%). Los pacientes que
recibieron ácido tióctico experimentaron menor dolor y sensación de ardor y parestesias,
y mejoría en el reflejo aquíleo y
sensibilidad al tacto (presión y punzadas).
Tratamiento de los factores
involucrados Neuropatía Diabética
Los avances en el conocimiento de la
fisiopatología del pie diabético y los factores involucrados han permitido
desarrollar diversas terapias prometedoras para evitar el avance de la lesión y
mejorar la calidad de vida del paciente.
La observación de un flujo excesivo de
metabolitos hacia la aldosa reductasa en la vía de los polioles abrió el camino
para la utilización de inhibidores de esta enzima.
Se considera que los inhibidores de la aldosa
reductasa reducen la desintegración del número de fibras nerviosas y la
distorsión de la morfología del nervio a largo plazo, al corregir los trastornos
metabólicos básicos de la vía del sorbitol y promover un ambiente más idóneo
para la restauración del nervio. Esta hipótesis se encuentra sometida a prueba
en numerosos ensayos clínicos prospectivos en pacientes con neuropatía
diabética.
Algunos ácidos grasos como el ácido γ-linoleico
(dosis de 300-500 mg diarios) y el ácido eicosapentaenoico (dosis de 1000-1500
mg diarios) han sido utilizados en pacientes con neuropatía sintomática
obteniéndose resultados controversiales.
En vista del alto grado de oxidación presente
en los pacientes diabéticos, se han utilizado antioxidantes como el ácido
lipoico. Algunos autores proponen que el tratamiento con este potente
antioxidante previene el desarrollo de la lesión neuronal y neurovascular en
personas con neuropatía diabética.
Por otro lado, la aplicación de oxígeno
hiperbárico para el manejo de pie diabético ha dado resultados contradictorios,
pues acelera la tasa de curación y reduce la necesidad de amputación de un pie
diabético con úlcera isquémica; sin embargo, la aplicación de una dosis
supra-terapéutica produce vasoconstricción debido a la pérdida de
vasodilatación estimulada por la hipoxia leve.
Además, la aplicación sistémica de oxígeno
hiperbárico puede causar problemas en el sistema nervioso central
Entre otros efectos secundarios, algunos
pacientes experimentan el desarrollo de cataratas, aumento significativo de la
miopía y fibroplasia retrolental -en especial- si las defensas antioxidantes
son precarias. A pesar del poco porcentaje de pacientes que presentan
“neuropatía hiperalgésica”, no debe olvidarse el manejo farmacológico adecuado
para esta condición con la finalidad de brindar alivio del dolor.
Los mismos pueden estar dirigidos a la
disminución de los niveles de glutamato o al aumento de los niveles de ácido
gamma-aminobutírico (GABA). En este orden de ideas, uno de los
medicamentos más utilizados es la gabapentina, un anticonvulsivante de segunda
generación utilizado principalmente en el tratamiento antiepiléptico, pero en
la actualidad se encuentra aprobado por la FDA (“Food and Drug Administration”)
para el dolor neuropático y aunque su mecanismo de acción no está del todo
esclarecido, se plantea que éste induce una reducción de la síntesis del
glutamato y un aumento de los niveles de GABA.
La pregabalina es otra droga recientemente
introducida en el armamentario contra la neuropatía dolorosa de la diabetes
Mellitus. Este medicamento es un análogo del GABA y aunque su mecanismo de
acción no está del todo claro, aparentemente exhibe su efecto analgésico
mediante la disminución de la liberación de neurotransmisores excitatorios como
el glutamato, aspartato, noradrenalina y sustancia P, debido a su fijación a la
subunidad alfa-2-delta de los canales de calcio voltaje dependientes (tipos N,
P y Q) que en el sistema nervioso central. De esta forma ocasiona una
disminución de la excitabilidad anormal en diferentes áreas del sistema
nervioso que guardan relación con el dolor, la epilepsia o la ansiedad. Está
indicado en el tratamiento del dolor neuropático periférico en adultos, en el
manejo de las crisis epilépticas parciales con o sin generalización secundaria
y en el trastorno de ansiedad generalizada.
La carbamazepina se mantiene como una buena
opción en el manejo del dolor neuropático. Sin embargo, su uso de forma crónica
está asociado con efectos indeseables como las dislipidemias, hiponatremia,
ganancia de peso, inducción de enzimas hepáticas, modificaciones, cambios en la
concentración de hormonas sexuales. Es estructuralmente similar a los
antidepresivos tricíclicos, y al igual que ellos tiene un efecto antagonista
sobre los canales de sodio. También es probable que tenga acción central y
periférica sobre los canales de adenosina, y puede inhibir la liberación de glutamato.
La oxcarbazepina es un derivado de la carbamazepina que comparte su acción analgésica,
aunque aparentemente con mejor perfil de seguridad.
A diferencia de los anticonvulsivos, los ADT
tienen una estructura química semejante y por ende comparten el mecanismo de
acción. Así, es menos razonable cambiar una droga por otra de esta clase cuando
el enfermo no responde en forma adecuada. No obstante, cada uno se asocia con
un perfil de seguridad distinto.
Amitriptilina e imipramina, clomipramina,
desipramina y doxepina son eficaces en dolor neuropático, independientemente
del efecto antidepresivo. Se considera que estos fármacos afectan numerosos
sitios en la vía del dolor, tanto a nivel central como periférico. La
amitriptilina, un antidepresivo tricíclico, que actúa inhibiendo la recaptación
de norepinefrina, ha mostrado reducir el dolor neuropático en pacientes
diabéticos. Sin embargo, su uso es limitado en estos pacientes, puesto que son
más susceptibles a sus efectos adversos, en especial aquellos con hipotensión
ortostática, retención urinaria y constipación.
Existen otros fármacos antidepresivos
denominados mixtos, ya que inhiben la recaptación de serotonina y
noradrenalina, tal es el caso de la duloxetina y la venlafaxina.
Según algunos estudios la acción de la
duloxetina es más rápida y posee menos efectos secundarios que la
amitriptilina. Actualmente se encuentra aprobado su uso para el tratamiento de
dolor neuropático en pacientes diabéticos adultos.
Un fármaco derivado del pimiento rojo picante
(capsaicina), ha sido aprobado por la FDA para el tratamiento de la neuralgia
post-herpértica y la neuropatía diabética, se piensa que su aplicación tópica
ocasiona depleción de los depósitos de sustancia P de manera reversible, así
como la de otros neurotransmisores en las terminaciones nerviosas, reduciendo
así la transmisión de la sensación dolorosa de los nervios periféricos a los
centros nerviosos.
DOLOR EN LA ENFERMEDAD VASCULAR
El dolor por isquemia es uno de los síntomas
importantes de la enfermedad vascular; en tanto, la claudicación se encuentra
en 3% de los hombres con edades o comprendidas entre los 45 y los 65 años y en
1% de las mujeres con edades entre 50 y 60 años. La arteriosclerosis es casi siempre el padecimiento
base en estos pacientes, que en su mayoría son diabéticos. En muchos individuos
que claudican, la causa de reducción del flujo es por obstrucción atero o
arteriosclerótica en el extremo proximal, la cual se combina con un grado
variable de anormalidades micro circulatorias, que quizá se exacerban por
efecto de los metabolitos anaeróbicos en los pequeños vasos.
EI tratamiento inicial para la circulación
incluye un programa de ejercicio, dejar de fumar y alivio o corrección
quirúrgica en la obstrucción proximal, si es posible una vez que se ponen en
práctica estas medidas, todavía restan numerosos pacientes con síntomas de
isquemia dolorosa en miembros y en algunos de ellos la simpatectomía química
lumbar resuelve el problema.
El tratamiento farmacológico del dolor por
isquemia periférica se puede dividir en varias categorías según los mecanismos
de acción que se buscan; éstos son:
• Los que detienen el progreso de la
arteriosclerosis
• Los que mejoran la circulación colateral
• Medicamentos que revierten las anormalidades
reológicas, los que impiden la trombosis y los que favorecen un buen
metabolismo hístico en la fase isquémica
Antilipidemicos
Se
sospecha que el colesterol y los triglicéridos son los causantes de la lesión
endotelial que desencadena los mecanismos aterógenos. No obstante que está
comprobado que estas sustancias pueden
manejarse de forma favorable mediante la farmacoterapia, se carece de certeza
en cuanto a que tal tratamiento produzca en efecto benéfico sintomático en el
dolor isquémico. De esta manera, el tratamiento con colestiramina y clofibrato de aluminio debe
reservarse para los casos en que sólo se trate de corregir los niveles séricos
de las sustancias mencionadas
Antiplaquetarios y
prostaglandinas
El efecto que se busca con estos dos fármacos
es inhibir en forma selectiva el Tromboxano A 2 plaquetario o reducir la
prostaciclina endógena elevada con Objeto de modificar el equilibrio de la
prostaglandina en favor del efecto antiadherente plaquetario y de la
vasodilatación; de esta manera se evitan la adherencia plaquetaria, el daño
endotelial y el progreso de la arteriesclerosis. La prostaglandina E-1 (PGE-1)
posee un poderoso efecto antiadherente sobre las plaquetas; se administra IV, a
veces en perfusión IV y, si no es efectiva en esta última forma, intraarterial
cada dos días o hasta a largo plazo. La PGE-1 es bastante eficaz en el
tratamiento de la claudicación intermitente no quirúrgica de las extremidades
inferiores y en el fenómeno de Raynaud. Aun cuando las venoclisis se
administran por periodos cortos, el efecto terapéutico puede prolongarse, lo
que sugiere que la PGE-1 posee cierto efecto tardío en el desarrollo de vasos
colaterales o detiene el avance de la enfermedad vascular básica. Sin embargo,
muchos afectados sufren recaidas y necesitan otra perfusión o un tratamiento
alternativo.
La PGI-2 (prostaciclina o epopronestol) es una sustancia que se encuentra de manera
natural en el endotelio, cuenta con un poderoso efecto plaquetario
antiadherente y vasodilatador, puede administrarse IV y suele darse por 3 dias consecutivos, aunque
el efecto suele durar más tiempo, hecho que contrasta con su vida media de unos
pocos minutos. Ello sugiere un efecto tardío sobre la aterogénesis o en la
formación de colaterales. Los efectos de la PGE-1 y PGI-2 son semejantes y se
resumen en la acción vasodilatadora que poseen; los principales efectos
secundarios son la hipotensión y la taquicardia y, en menor grado, bochornos,
fiebre, cefalea y arritmias cardiacas mínimas, efectos que en ocasiones obligan
a discontinuar el tratamiento.
Ácido acetilsalicílico
Es un inhibidor de la ciclooxigenasa
plaquetaria, por lo que reduce la cantidad de tromboxano A-2, inclinando así el
nivel de prostaglandinas hacia un mayor efecto de la prostaciclina. A dosis
bajas de 5 mg x kg x día la aspirina puede modificar de manera favorable el
dolor de la isquemia; en tanto, no hay evidencia convincente de que la adición
de dipiridamol o de sulfinpirazona proporcione efectos benéficos agregados.
Deben evitarse las dosis más altas del ácido acetilsalicílico (mayores de 10 mg
x kg x día) ya que pueden presentarse efectos adversos, los principales de los
cuales son una gastritis erosiva o hemorragia intestinal o úlcera gástrica.
Medicamentos que favorecen la
circulación colateral (AMG, 1999)
Vasodilatadores
El empleo de vasodilatadores en el tratamiento
de dolor isquémico se basa en dos hipótesis; la primera acepta que estos
pacientes presentan algún vasoespasmo y la segunda supone que la circulación
colateral se abre con vasodilatadores. Por desgracia, no se cuenta con
evidencia de que los vasodilatadores disponibles en la actualidad tengan un
efecto que se relacione con dichas hipótesis. Los relajantes de la musculatura
lisa con acción vascular son ineficaces, como la papaverina, ácido nicotínico,
cinaricina y ciclandelato. De igual manera, los vasodilatadores de mediación
neural han resultado inútiles en este contexto y entre éstos se incluyen los
antagonistas adrenérgicos beta como isoxsuprina y nilidrina, antagonistas
adrenérgicos alfa como la fenoxibenzamina, timoxamina y tolazolina, así como
los agotadores de catecolaminas guanetidina y reserpina.
Medicamentos para revertir las
anormalidades reológicas (AMG,
1999)
Los eritrocitos normales con diámetro de 8 a 9
micras pueden pasar a través de los capilares en la microcirculación, no
obstante que estos capilares apenas alcanzan 4 o 5 micras de diámetro. Para
comprender cómo ocurre lo anterior ha de recordarse que las células rojas
sufren notable deformación en varias situaciones (p ej., anemia falciforme,
deficiencias de hierro, aterosclerosis). El hematocrito muestra relación
inversa con la viscosidad sanguínea; de esta manera es posible que un exceso
de glóbulos rojos o de células muy rígidas
incremente la deficiencia micro circulatoria y agrave la isquemia. Los agentes
hemorreologicos son de gran utilidad para revertir la patología y con ello reducir el dolor de la isquemia.
La pentoxifilina disminuye la viscosidad
sanguínea, sobre todo al aumentar la capacidad de deformación de los glóbulos
rojos, pero también al aminorar el fibrinógeno plasmático y la adherencia
plaquetaria. Algunos estudios controlados demuestran que existe una definitiva
(aunque modesta) mejoría en la claudicación cuando se emplea este medicamento
por vía oral a dosis de 600 a 1 200 mg por día, en comparación con placebo,
adenosina, nilhidrina. Los efectos adversos por lo general son moderados e
incluyen náuseas, vómito y somnolencia. En tan solo 3 % de los pacientes estas
molestias llegaron a ser de tal grado intensas que fue necesario suspender el
tratamiento.
Un nuevo fármaco, la ketanserina, parece tener
efecto vasodilatador, hemorreológico y antiadherente plaquetario. Podría
convertirse en un importante medio para tratar el dolor isquémico, pero por el
un momento se encuentra en fase de investigación.
Los dextranos actúan como hemo diluyentes y
disminuyen la viscosidad sanguínea, pero como carecen de efecto duradero no
resultan prácticos en pacientes con dolor de esta naturaleza.
La terapéutica fibrinolítica con esteroides
anabólicos (del tipo estanozol) también suele tener acción limitada,
pero sus efectos adversos sobrepasan los beneficios.
Medicamentos para revertir o
prevenir la trombosis(AMG, 1999)
Si se
tiene en consideración que la trombosis mural es quizás el desenlace de lo
arteriosclerosis, resultaría lógico intentar la prevención o aun la reversión
de la trombosis, una vez que se establece.
En los casos inoperables con isquemia aguda de
miembros, el tratamiento trombolítico con estreptocinasa o urocinasa
intraarteriales ofrece resultados preventivos al evitar la pérdida del miembro
afectado, pero no es un tratamiento practico para aliviar el dolor isquémico
por un periodo prolongado.
Los antagonistas de la vitamina K (warfarina
sódica o cumadina) favorecen la producción de hipoprotrombinemia con fines
terapéuticos, aunque carecen de efectos para aliviar el dolor por isquemia.
Medicamentos que mejoran el metabolismo hístico en los
estados isquémicos
Si llegan a fracasar todos los esfuerzos por
restablecer una circulación efectiva, debe recurrir a una medida más: facilitar
la función hística en un estado isquémico.
Se sabe que durante la isquemia un tejido
puede ser atacado parcialmente por un radical libre de oxígeno que daña las membranas lípidas. Esto
es en particular cierto cuando a los
periodos de isquemia les siguen intervalos de reperfusión. Durante la
isquemia se forma hipoxantina a partir del trifosfato de adenosina (ATP),
en tanto que la enzima xantinooxidasa se origina a partir de su
precursora, la deshidrogenasa de xantina, mediante la acción de una xantina
dependiente de calcio. Tras la perfusión, el oxígeno molecular actúa sobre la
hipoxantina por medio de la enzima xantinooxidasa y ocasiona la ruptura
del radical superóxido Algo semejante ocurre durante la inflamación. El dolor
durante este proceso y durante la reperfusión de la isquemia puede relacionarse
con las acciones citotóxicas de los radicales libres de oxígeno; si es así,
esta cadena puede interrumpirse en varios de sus eslabones. Un bloqueador del
canal del calcio podría obstruir la formación de la proteasa dependiente del
mismo, generada en concentraciones suficientes para catalizar la producción de
xantinooxidasa. Un inhibidor de esta última disminuye la reacción entre la
hipoxantina y el oxígeno molecular durante la reperfusión. Un arrasador de
radicales libres puede neutralizar el radical superóxido antes que peroxide las
membranas lípidas.
Los bloqueadores del canal del calcio casi
siempre están disponibles, aunque no se han probado en pacientes con dolor
isquémico en la medida suficiente como para recomendar su empleo en esta
eventualidad. Los bloqueadores verapamil, nifedipina y nimodipina poseen efecto
vasodilatador. El alopurinol, un inhibidor de la xantinooxidasa, reduce el daño
por reperfusión y tal vez así sea eficaz para tratar el dolor por isquemia. La
enzima dismustasa de superóxido, la catalasa y muchos otros radicales libres
depuradores han demostrado también su poder para reducir el daño de la
reperfusión, pero hasta ahora no existen datos acerca de su eficacia clínica en
casos de dolor por isquemia.






No hay comentarios.:
Publicar un comentario