Objetivos
Al finalizar la
lectura de este artículo, el lector podrá:
Conocer
otras enfermedades del apéndice cecal
Mapa
conceptual
Otras enfermedades del apéndice
La enfermedad
de Crohn causa sólo el 5-10% de las apendicitis granulomatosas; en este caso
existen habitualmente otras lesiones digestivas de la enfermedad (en la
apendicectomía suele indicarse una ileocolonoscopia) (Bronner, 2004).
Rara vez puede deberse a una sarcoidosis, una reacción a cuerpos extraños, una
infección micobacteriana, fúngica o
parasitaria o, sobre todo, por Yersinia
enterocolitica. La causa más frecuente sería una apendicitis aguda o
subaguda recidivante y el tratamiento es la apendicectomía.
Divertículo
En forma ocasional se
observa un divertículo o una diverticulosis del apéndice. El cuadro ha sido
documentado en detalle por Wilson.
Intususcepción
La intususcepción del
apéndice es rara y se han comunicado sólo alrededor de 160 casos desde que
McKidd describió el primer ejemplo en 1858.
La intususcepción puede comenzar en el extremo
o en la base del apéndice y en ambos casos el resultado final es la inversión
completa dentro del ciego. En la mayoría de los pacientes registrados, la
intususcepción era de la forma simple (es decir, inversión dentro del ciego),
pero en algunos la inversión apendicular se asoció con intususcepción
cecocólica o ileocólica. Con poca frecuencia se ha detectado un apéndice
intususcepcionado por examen rectal.
Habitualmente es posible reducir la
intususcepción por manipulación quirúrgica. Una vez realizada la reducción, el
apéndice se extirpa de la forma habitual. Si no es posible realizar la
reducción, se efectúa una resección local con anastomosis ileocólica. (Maingot
20 . Shakelfort)
Torsión
La torsión del apéndice fue descrita por
primera vez por Payne en 1918. Desde entonces, se han comunicado sólo unos
pocos casos. En la mayoría de ellos el apéndice se encontraba en posición
pelviana y había sufrido torsión en sentido antihorario. Los factores
etiológicos son desconocidos, pero se han considerado como tales la presencia
de un mesoapéndice laxo, en forma de abanico, así como de cuerpos extraños en
el apéndice. Los signos y síntomas son los de la apendicitis aguda y el
tratamiento es una apendicectomía.
Endometriosis
El apéndice está afectado en < 1 % de los
casos de endometriosis pelviana. Raramente está comprometido sólo el apéndice. La existencia de tumores apendiculares y su
carácter, a veces inaccesible a la exploración macroscópica, justifican
ampliamente la exploración anatomopatológica sistemática de todo apéndice
extraído, independientemente de su estado inflamatorio.
Parásitos apendiculares
Varios parásitos intestinales
causan apendicitis. Si bien el más común es Ascaris lumbricoides, se
relaciona una amplia gama de helmintos que incluyen Enterobius vermicularis,
Strongyloides stercoralis y Echinococcus granulosus. Los
parásitos vivos ocluyen la luz del apéndice y causan obstrucción. La presencia
de parásitos en el apéndice durante la operación dificulta en términos técnicos
la ligadura y engrapado del apéndice. Una vez que se practicó la apendicectomía
y se recuperó el sujeto, se requiere tratamiento con helminticidas para
desparasitar el resto del tubo digestivo. La amebosis también puede ocasionar
apendicitis. La invasión de la mucosa por trofozoítos de Entamoeba
histolytica suscita un proceso inflamatorio intenso. La afección
apendicular es un componente de la amebosis intestinal más generalizada.
Después de la apendicectomía es necesario administrar el tratamiento
antimicrobiano apropiado (metronidazol).
Tumores neuroendocrinos apendiculares (antes denominados
carcinoides) (Thesaurus)
Suelen ser de hallazgo fortuito en
una pieza de apendicectomía. Todo se basa en el estudio sistemático de la pieza
quirúrgica. Los tumores del apéndice
son inusuales, lo que puede deberse a la pequeña superficie de la mucosa
disponible rara la alteración maligna. Por lo tanto, este órgano tiene
probablemente la misma chance de desarrollar un cáncer que cualquier otra parte
del intestino grueso, del cual representa un anexo. Son
en extremo raras las afecciones malignas apendiculares. Se diagnostica cáncer
apendicular primario en 0.9 a 1.4% de los especímenes de apendicectomías. Sólo en contadas ocasiones se sospechan estos
tumores antes de la intervención. Menos de 50% de los casos se diagnostica en
la operación.
Es cierto, sin embargo, que la distribución de
los tipos de tumor contrasta con la del resto del intestino grueso. Por lejos, la neoplasia más frecuente del
apéndice es el tumor carcinoide, que representa el 85% de todos los tumores de
este órgano y que se encuentra en alrededor del 0,1% de todos los apéndices
sometidos a examen histológico cuidadoso. Como sucede en el resto del intestino
grueso, también pueden observarse tumores vellosos y carcinomas.
Los tumores benignos del apéndice son raros, e
incluyen pólipos adenomatosos, cistadenoma mucoso, leiomioma, fibroma y
neuroma. El cistadenoma mucoso, aunque poco frecuente, puede obstruir la luz
del apéndice y distenderla con mucus para formar un mucocele. Las otras
lesiones benignas, debido a que se desarrollan en la pared del apéndice, no
obstruyen la luz, raramente tienen importancia clínica y en general se detectan
sólo como observación accidental en una pieza de apendicectomía o post mortem.
Sin embargo, en una revisión
reciente del programa del National Cancer Institute’s Surveillance,
Epidemiology and End Results (SEER) se encontró una incidencia de
afecciones apendiculares ajustada a la edad de 0.12 casos por 1 000 000 de
personas por año. Los datos del programa SEER identificaron al adenocarcinoma
mucinoso como el diagnóstico histológico más frecuente (38% del total de casos
publicados), seguido de adenocarcinoma (26%), carcinoide (17%), carcinoma de
células caliciformes (15%) y carcinoma de células en anillo de sello (4%). La
supervivencia a cinco años para los tumores malignos apendiculares varía según
el tipo de lesión. Los pacientes con tumores carcinoides tienen la mejor
supervivencia a cinco años (83%), mientras que aquéllos con carcinoma de
células en anillo de sello tienen la más pobre (18%). (Schwartz, Maingot)
El seguimiento es inútil en caso
de tumor de menos de 1cm (o de menos de 2 cm sin invasión de la base del
apéndice) en ausencia de metástasis ganglionares, de émbolos venosos o
linfáticos en el mesoapéndice, de invasión del mesoapéndice de más de 3mm y de
elemento adenocarcinomatoso («adenocarcinoide»). En los casos dudosos se
necesita la opinión de un experto (Grozinsky, 2013). En los demás
casos se indica una hemicolectomía derecha, precedida de una valoración amplia
y seguida de una vigilancia regular.
Tumores mucinosos apendiculares (Sugarbaker,
2009)
A
Rokitansky se le atribuye la primera descripción de esta entidad en 1842. Descubiertos en una pieza
quirúrgica de apendicectomía necesitan (excepto el carcinoma in situ
intraepitelial), según el grado histológico, una resección ileocecal o una
hemicolectomía derecha.
El mucocele
apendicular se define por su aspecto macroscópico: el apéndice aumentado de
tamaño es llenado por el moco que secreta un tumor mucinoso bien diferenciado y
habitualmente maligno
Un mucocele apendicular da lugar
al crecimiento progresivo del apéndice por acumulación intraluminal de una
sustancia mucoide. Los mucoceles pueden generarse por uno de cuatro procesos:
quistes de retención, hiperplasia mucosa, cistadenomas y cistadenocarcinomas..
El mucocele del apéndice ocurre en formas
obstructivas, benignas y malignas. En la forma obstructiva existe obstrucción
de la luz del apéndice y acumulación de mucus distal a la obstrucción. Las
características clínicas clásicas del mucocele obstructivo incluyen malestar y
masa palpable en la fosa ilíaca derecha y hallazgos radiográficos de defecto de
relleno en el ciego sin visualización del apéndice. Cuando se descubre esta
lesión en el momento de una laparotomía exploradora por sospecha de apendicitis
aguda debe realizarse una apendicectomía simple.
La variedad neoplásica del
mucocele ocurre por distensión de la luz del apéndice por el mucus secretado
por la proliferación de células tumorales. La forma benigna es el cistadenoma
mucinoso y la forma maligna el cistadenocarcinoma mucinoso. Debido a que es
difícil distinguir entre los tumores benignos y malignos se debe realizar una
hemicolectomía derecha, ya que en los casos usuales la apendicectomía no es
curativa. Cuando existen numerosos implantes peritoneales de una sustancia
similar a la mucina es apropiado el diagnóstico de seudomixoma peritoneal.
Dentro de estas masas gelatinosas existen nidos de células tumorales adheridas
al peritoneo.
Hay que prestar mucha atención a
no romper el apéndice (riesgo de diseminación peritoneal) y a efectuar un
estudio citológico peritoneal. En ausencia de invasión de los márgenes, del
mesoapéndice, de signos de malignidad histológica y de citología peritoneal
positiva, se indica una vigilancia anual. Si no, el caso debe discutirse en
reunión de concertación multidisciplinar especializada (colectomía derecha,
discusión de quimiohipertermia intraperitoneal). El mucocele apendicular
maligno es la causa principal del seudomixoma peritoneal (enfermedad gelatinosa
del peritoneo).
En el
estudio histológico los mucoceles se dividen en tipo benigno, que se debe a
oclusión no inflamatoria de la luz próximal del apéndice y en consecuencia no
es una neoplasia, y tipo maligno, que es un adenocarcinoma papilar mucoso grado
I. El tratamiento adecuado es una apendectomía, pero es necesario tener cuidado
para evitar romperlo ya que se ha observado seudomixoma peritoneal consecutivo
a rotura y diseminación peritoneal del contenido apendicular.
Es posible que haya tumores mucinosos del
ovario sincrónicos con los apendiculares. La frecuencia de bilateralidad de la
afección ovárica, con predominancia del lado derecho, sugiere que las
neoplasias del ovario son secundarias. El tratamiento consiste en apendectomía
u ooforectomía bilateral si están invadidos ambos ovarios e histerectomía.
La dilatación quística de un apéndice
relleno de moco (0,3 % de la apendicectomías) es una entidad a menudo
clasificada en la frontera de la malignidad. Los criterios de ésta se basan en
la presencia de células epiteliales en los lagos mucosos. 4 subtipos: 1.
Quistes de retención, 2. hiperplasia mucosa, 3. cistadenoma y 4.
Cistadenocarcinoma .
El Mucocele de la apéndice se
divide en 4 entidades patológicas distintas:
1. mucocele no neoplásico debido a obstrucción luminal;
2.
la hiperplasia de la mucosa;
3.
cistoadenoma mucinoso con
cambio a adenomatosa velloso; y
4. cystadenoma maligno mucinoso.
Estas lesiones pueden producir una ascitis refractaria, que tiene ha
referido como seudomixoma peritoneal.
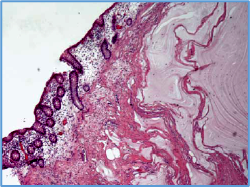
Figura : Histológicamente áreas tanto de hiperplasia de la mucosa y atrofia. Había extravasación de mucina en la pared del apéndice . esta extravasación carecía de células.
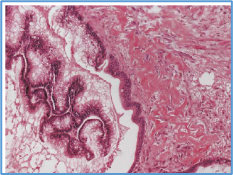
Figura: epitelio columnar estratificado Atípico
consistente con el diagnóstico de un cistoadenoma. Moco
presente en luz del apéndice (izquierda).
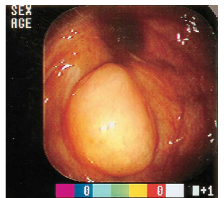
Figura La visión endoscópica del mucocele. La colonoscopia
puede revelar en la base del ciego una
suave hinchazón hemisférica cubierta por
mucosa normal
El
primer informe de un diagnóstico por colonoscopia fue de Ponsky en 1976. En el
tratamiento quirúrgico es necesario confirmar el diagnóstico para evitar la complicación de pseudomixoma
peritoneal que pueden seguir a la perforación de un mucocele si la patología
primaria es un cistoadenoma o cystadenocarcinoma
El cuadro clínico del mucocele es inespecífico, a menudo es un
hallazgo incidental en la operación para apendicitis aguda. Un mucocele intacto
no representa un riesgo futuro para el paciente, pero ocurre lo contrario si el
mucocele se rompe y las células epiteliales escapan hacia la cavidad
peritoneal. Como resultado, cuando se encuentra un mucocele durante una
exploración laparoscópica, se recomienda la conversión a laparotomía abierta.
La conversión de una técnica laparoscópica a una laparotomía asegura que un
proceso benigno no se transforme en uno maligno por la rotura de un mucocele.
Además, la laparotomía permite la exploración abdominal minuciosa para
descartar la presencia de acumulaciones de líquido mucoide. La presencia de un
mucocele en el apéndice no obliga a practicar una hemicolectomía derecha. Los
principios quirúrgicos incluyen resección
del apéndice, resección amplia del mesoapéndice para incluir todos los
ganglios linfáticos apendiculares, recolección y examen citológico de todo moco
intraperitoneal e inspección cuidadosa de la base del apéndice. La
hemicolectomía derecha, o de preferencia la extirpación del ciego, se reserva
para pacientes con margen positivo en la base del apéndice o ganglios
linfáticos periapendiculares positivos. En fecha reciente se sugirió una
estrategia más agresiva para las neoplasias apendiculares rotas. Esta
estrategia incluye una técnica minuciosa, pero de agresividad mínima, en la
laparotomía inicial, como se describió antes, con referencia ulterior a un centro
especializado para considerar una nueva exploración con quimioterapia
intraperitoneal hipertérmica.
Tumor carcinoide
Los carcinoides apendiculares son tumores
neuroendocrinos constituidos habitualmente por celulas enterocromafines. A
menudo contienen celulas sustentaculares que expresan S-100. Aunque se
clasifican como neoplasias malignas, la mayoria de los carcinoides apendiculares demuestran un
comportamiento benigno.
Casi siempre es un hallazgo solitario, aunque
en ocasiones puede asociarse con carcinoides del íleon.
El hallazgo de una masa bulbar,
amarilla y dura en el apéndice debe despertar la sospecha de un carcinoide
apendicular. El apéndice es el sitio más común de carcinoide gastrointestinal,
seguido del intestino delgado y a continuación el recto. El síndrome carcinoide
rara vez se vincula con un carcinoide apendicular, a menos que existan
metástasis diseminadas, que ocurren en 2.9% de los pacientes. Son raros los
síntomas atribuibles de forma directa al carcinoide, aunque en ocasiones el
tumor puede obstruir la luz apendicular en forma muy similar a un fecalito y
provocar apendicitis aguda.
Casi todos los carcinoides se
hallan en la punta del apéndice. El potencial de malignidad se relaciona con el
tamaño y los tumores menores de 1 cm rara vez se extienden fuera del apéndice o
adyacentes a la masa. El tamaño promedio de los tumores carcinoides es 2.5
cm.100 Los carcinoides casi siempre se manifiestan con enfermedad localizada
(64%). El tratamiento para los tumores ≤1 cm es la
apendicectomía. Para tumores mayores de 1 a 2 cm situados en la base o con
metástasis a ganglios linfáticos está indicada la hemicolectomía. A pesar de
estas recomendaciones, los datos de SEER indican que al menos en 28% de las
ocasiones no se practica la operación adecuada para los carcinoides.
El tratamiento adecuado consiste en
apendectomía simple con excisión amplia del mesoapéndice, a menos que se
compruebe una invasión más allá de la línea de resección, metástasis
ganglionares o ambos, en cuyo caso está indicada una colectomía derecha con excisión
del mesenterio que aloja ganglios.
Figura. Algoritmo para el tratamiento de pacientez con carcinoide apendicular. Tomado d e Brunicardi, 2014.
Los adenocarcinoides, que
comparten características morfológicas y clínicas que incluyen una combinación
de adenocarcinomas y carcinoides, son raros. Si hay atipia nuclear moderada o
intensa está indicado el tratamiento por hemicolectomía derecha. Si no existe,
una apendectomía simple resulta adecuada.
Anatomía patológica
Los tumores carcinoides se
originan en las células argentafines, que se encuentran localizadas en las
bases de las criptas de la mucosa intestinal. Estas células a menudo se
denominan células de Kulchitsky, en honor del histólogo que hizo la descripción
original. Característicamente contienen granulos que toman las tinciones de
plata en su citoplasma; de donde surge el nombre alternativo argentafinoma.
A simple vista, el tumor
forma un nodulo duro y amarillo grisáceo en el apéndice que se origina en las
profundidades de la mucosa, con un diámetro que oscila entre 0,5 y 3,5 cm. En
el examen microscópico, la pared muscular está invadida y en muchos casos está
comprometido el peritoneo que lo recubre. Sin embargo, la diseminación
metastásica es rara. En el estudio realizado por Moertel y col., se encontraron
metástasis sólo en el 1,4% de los casos y se limitaron prácticamente a lesiones
>2 cm de diámetro. Estos tumores fueron responsables de solamente el 1% de
los carcinoides de apéndice. En el estudio realizado por Svendsen y Bülow que
incluyó 64 pacientes de menos de 40 años con tumores carcinoides del apéndice,
sólo un individuo tuvo metástasis locales y en este caso el tumor medía 2 cm de
diámetro. Anderson y Wilson estudiaron 147 pacientes con tumores carcinoides
del apéndice. Dos de éstos presentaron diseminación metastásica en el momento
de la presentación y ambos tenían tumores >2 cm de diámetro. Parkes y col.
revisaron 40 niños con este cuadro, menores de 15 años. Todos los tumores
fueron hallazgos accidentales. No se registraron recidivas, metástasis ni
muertes. Estos autores estiman una incidencia del 0,08% en las apendicectomías
realizadas en niños o sea una tasa de 1,14 por millón de niños por año.
La mayoría de los
carcinoides se encuentran accidentalmente en estudios histológicos de rutina de
apéndices extirpados en el curso de una laparotomía por otras razones. Debido a
la localización habitual del tumor en el extremo del apéndice, en general no se
desarrolla apendicitis. Sin embargo, la luz puede estar ocluida por un tumor de
la base o del cuerpo y en ese caso, el carcinoide puede presentarse como una
apendicitis aguda o incluso como un absceso apendicular
El síndrome carcinoide, que
es el resultado de la secreción de 5-hidroxitriptamina dentro de circulación
portal, se ve solamente en casos de carcinoide extensivo maligno, casi siempre
asociado con metástasis hepáticas. En estas circunstancias, el apéndice
raramente es la localización del tumor primitivo, que en general se encuentra
en el íleon terminal
Adenocarcinoma
El primer caso de carcinoma
del apéndice fue descrito por Berger en 1882. Menon, en un trabajo de 1980
sobre dos casos que se presentaron como masas apendiculares, pudo encontrar
menos de 200 ejemplos en publicaciones en idioma inglés y presentó una valiosa
revisión clínica del tema. Gilhome y col. hallaron sólo 10 ejemplos confirmados
entre 9.380 apéndices enviados a anatomía patológica, en tanto que Burgess y
Done encontraron 11 carcinomas en 10.526 apendicectomías, 8 de los cuales
fueron extirpados como emergencias y tres por operaciones programadas.
El aspecto histológico del
adenocarcinoma de apéndice es similar al de estos tumores en otras
localizaciones del intestino grueso, excepto en que la secreción mucosa es un
poco más intensa. La lesión puede ser polipoide o ulcerada y puede producir
hemorragias u obstrucción de este órgano. Típicamente, el tumor se origina en
la base del apéndice en pacientes de más de 50 años. Puede ser un hallazgo
accidental o puede ser confundido con una apendicitis aguda o un absceso
apendicular. Si el tumor invade el ciego, puede ser difícil diferenciarlo de un
carcinoma primitivo de origen cecal.
El adenocarcinoma primario del
apéndice es una neoplasia rara de tres subtipos histológicos principales:
adenocarcinoma mucinoide, adenocarcinoma de colon y adenocarcinoide. La forma
de presentación más común del carcinoma apendicular es la de una apendicitis
aguda. Los pacientes también pueden presentar ascitis o una masa palpable o es
posible que se descubra la neoplasia durante un proceso quirúrgico por alguna
causa no relacionada.
Figura : Adenocarcinoma se
muestra el llenado del lumen del apéndice. Histológicamente la lesión era un
adenocarcinoma mucinoso moderadamente diferenciado.
El tratamiento que se recomienda en todos los individuos con adenocarcinoma del apéndice es una hemicolectomía derecha formal. Los adenocarcinomas apendiculares muestran una propensión a perforarse en fases tempranas, aunque no se vincula con claridad con peores pronósticos. La supervivencia total a cinco años es de 55% y varía con la etapa y el grado. Los sujetos con adenocarcinoma apendicular tienen un riesgo considerable de neoplasias sincrónicas y metacrónicas, de las cuales cerca de la mitad se origina en el tubo digestivo.
A veces el diagnóstico no se establece hasta el examen posoperatorio de la pieza. Si se encuentra un tumor carcinoide y la resección ha sido adecuada, no es necesario realizar ningún procedimiento adicional. Si el carcinoide afecta la base del apéndice y el examen histológico muéstra que la resección ha sido incompleta, por cierto está indicado reoperar, con escisión de un adecuado manguito de pared cecal circundante. Si la pieza muestra la presencia de un indudable adenocarcinoma, aunque la resección haya sido adecuada, se debe aconsejar al paciente que se someta a una hemicolectomía derecha formal.
Tumores vellosos
Los tumores vellosos del apéndice pueden ser papilares o adenomatosos. La mayoría son no invasores, pero tienen propensión a llenar el apéndice con mucus, lo que hace difícil su diferenciación de un mucocele benigno. Si no se rompen, los tumores raramente producen metástasis, pero la perforación de un mucocele maligno puede dar como resultado un seudomixoma peritoneo.
Los tumores vellosos apendiculares, cuyo hallazgo es fortuito y su diagnóstico siempre secundario; su tratamiento se limita a la apendicectomía; si se demuestra su degeneración histológica, especialmente si existe una invasión de la base apendicular, también se indica la hemicolectomía derecha secundaria;
Linfoma
El linfoma del apéndice es en extremo raro. El tubo digestivo es el sitio extraganglionar que se afecta con mayor frecuencia con linfoma del tipo no Hodgkin. También se han comunicado otros tipos de linfoma, como el de Burkitt y la leucemia. La frecuencia de linfoma primario del apéndice varía de 1 a 3% de los linfomas gastrointestinales. El linfoma apendicular aparece en la forma de una apendicitis aguda y rara vez se sospecha antes de la intervención. Los hallazgos en la CT de un diámetro apendicular de 2.5 cm o mayor o engrosamiento del tejido blando circundante deben llevar a sospechar un linfoma apendicular. El tratamiento del linfoma apendicular limitado al apéndice es la apendicectomía. Está indicada una hemicolectomía derecha cuando el tumor se extiende más allá del apéndice al ciego o al mesenterio. Antes de iniciar el tratamiento coadyuvante se solicita un estudio posoperatorio para asignar la etapa. En el linfoma limitado al apéndice no está indicado tratamiento coadyuvante.
Seudomixoma peritoneal
El seudomixoma peritoneal es un trastorno raro en el que acumulaciones difusas de líquido gelatinoso se acompañan de implantes mucinosos en las superficies peritoneales y el epiplón. El seudomixoma es dos a tres veces más común en mujeres. Estudios inmunocitológicos y moleculares recientes sugieren que el apéndice es el sitio de origen de la mayor parte de los casos de seudomixoma. Este último se debe de manera invariable a células neoplásicas que secretan moco dentro del peritoneo. Puede ser difícil clasificar estas células como malignas porque pueden ser escasas, estar diseminadas de modo extenso y tener un aspecto citológico de grado bajo. Los sujetos con seudomixoma sufren dolor, distensión o una masa abdominales. El seudomixoma primario no provoca disfunción de órganos abdominales. Sin embargo, es posible observar obstrucción ureteral y del retorno venoso. El seudomixoma es una lesión que progresa despacio y cuyas recurrencias pueden tardar años en desarrollarse o causar síntomas. En una serie de la Clínica Mayo, 76% de los pacientes desarrolló recurrencias abdominales. Las metástasis ganglionares y distantes son infrecuentes.
El uso de imágenes antes de la operación tiene ventajas para planear la intervención quirúrgica. La modalidad de imágenes preferida es la CT. Durante la operación se encuentra un volumen variable de ascitis mucinosa junto con depósitos tumorales que incluyen el hemidiafragma derecho, el espacio retrohepático derecho, la escotadura paracólica izquierda, el ligamento de Treitz y los ovarios en mujeres. Por lo general, las superficies peritoneales del intestino no están afectadas por el tumor. El aspecto fundamental del tratamiento es una citorreducción quirúrgica amplia. Debe extirparse todo el tejido visible y el epiplón. De no realizar lo anterior, debe practicarse de rutina una apendicectomía. En mujeres se efectúa una histerectomía con salpingooforectomía bilateral. La supervivencia es mejor en pacientes que se someten a resección R0 o R1 que en pacientes con resección R2 (enfermedad macroscópica residual). Como la supervivencia a cinco años para las neoplasias apendiculares mucinosas es de sólo 30%, se sugiere la quimioterapia hipertérmica intraperitoneal adyuvante como adjunto estándar a la cirugía citorreductora radical. La cirugía citorreductora con quimioterapia hipertérmica intraperitoneal es un procedimiento largo y tedioso con tiempos quirúrgicos publicados de 300 a 1 020 min. Además, la morbilidad (38%) y mortalidad (6%) son altas. La cirugía citorreductora con quimioterapia hipertérmica intraperitoneal se relaciona con una supervivencia a cinco años de 53 a 78%. La supervivencia se vincula con el estado de desempeño inicial del paciente. Cualquier recurrencia debe investigarse de modo exhaustivo. Las recurrencias se tratan con una operación adicional. Es importante señalar que la operación de la enfermedad recurrente es difícil y se acompaña de una frecuencia mayor de enterotomías, fístulas anastomóticas y fístulas involuntarias.


No hay comentarios.:
Publicar un comentario