COLECISTECTOMÍA
LAPAROSCÓPICA.
Dr. Juan Hernandez Orduña.
En
el año 1882, el cirujano
alemán Carl Langenbuch llevó a cabo la primera extirpación de la vesícula biliar mediante laparotomía.
En 1987, Philippe Mouret utilizó por primera vez en Lyon la laparoscopia para realizar una colecistectomía. Esta técnica respondía a los esfuerzos por reducir
la vía de acceso
necesaria para realizar esta operación: incisión media supraumbilical, después incisión subcostal derecha, seguida de minilaparotomía, así como las consecuencias funcionales postoperatorias relacionadas con esta vía de acceso. En la actualidad, todas las operaciones de cirugía abdominal se realizan en parte, o completamente, mediante laparoscopia. Entre las fuerzas que han contribuido a la magnífica difusión de esta técnica,
no hay que olvidar que quizás coincide
con el deseo o la necesidad
de responder de forma cada vez más imperativa a las esperanzas explícitas e implícitas
del «paciente cliente
». La laparoscopia no es más que una vía de acceso, y a través de la
experiencia adquirida con esta técnica, los cirujanos
han tomado conciencia de que una gran parte de las consecuencias dolorosas o funcionales postoperatorias inmediatas
dependía de la vía de acceso, más
que
de la operación
a la que había dado pasó.
La litiasis biliar se transforma en enfermedad cuando
los cálculos de la vesícula son sintomáticos o migran fuera de la vesícula al conducto colédoco. Este capítulo está dedicado al tratamiento quirúrgico de la litiasis biliar sintomática con la ayuda de la laparoscopia. La finalidad no es sólo extirpar
la vesícula, sino diagnosticar y tratar la enfermedad litiásica en su conjunto.
La complicación más grave de la colecistectomía es la lesión del colédoco.
La frecuencia y la gravedad de estas lesiones
han sido y siguen siendo
muy altas con la técnica
laparoscópica, y sobre todo lo fueron en las primeras
intervenciones.
La laparoscopia ha «creado» el término
de curva de aprendizaje. Todos los medios
diagnósticos y técnicas
necesarias para prevenir
y diagnosticar esta complicación deben ser considerados como prioritarios.
Dado que la colecistectomía es la operación laparoscópica más frecuente realizada por los cirujanos generales y digestivos, los principios técnicos generales de la laparoscopia en sí ocupan aquí un lugar amplio.
Indicación quirúrgica
La litiasis vesicular sintomática y/o complicada (colecistitis aguda, colecistitis escleroatrófica, migración litiásica coledocal, etc.) constituye una indicación formal de colecistectomía. Sólo la presencia
de factores de riesgo generales (cardiorrespiratorios, coagulopatía) puede
cuestionar la indicación quirúrgica. Varias
conferencias internacionales de consenso
han establecido la indicación de colecistectomía laparoscópica como la intervención de referencia en la litiasis
vesicular sintomática (Neugebauer, 2000).
Las contraindicaciones formales del abordaje laparoscópico son, respecto al paciente, la sospecha
de un cáncer de vesícula
Contraindicaciones formales del abordaje laparoscópico
1.
Sospecha de cáncer de vesícula.
2.
Cirujano sin experiencia en cirugía
laparoscópica.
3.
y, en lo que respecta
al cirujano, la falta de experiencia específica en cirugía
laparoscópica o del instrumental adecuado.
Las contraindicaciones absolutas de la colecistectomía laparoscópica son las hemodinámicas o las respiratorias del neumoperitoneo.
Un abdomen con múltiples adherencias, procesos inflamatorios agudos, colecistitis supurada, colecistitis gangrenosa, fístulas biliodigestivas o cirrosis
con hipertensión portal dificultarán el procedimiento quirúrgico. Sin embargo, en la actualidad la mayoría
de los cirujanos que cuentan
con una experiencia significativa en cirugía
laparoscópica exploran a todos los pacientes
a través de esta vía,
con la posibilidad de conversión si es necesario.
Situaciones difíciles en laparoscopia
•
Abdomen con múltiples intervenciones quirúrgicas y varias adherencias.
•
Procesos inflamatorios significativos (colecistitis supurada,
etc.)
•
Fístulas biliodigestivas.
•
Cirrosis con hipertensión portal.
Es preciso obtener un consentimiento informado preoperatorio tras explicar las ventajas, las complicaciones del abordaje
laparoscópico y las circunstancias y los beneficios de la conversión en laparotomía en caso de una intervención difícil.
La conversión
debe ser considerada por el cirujano
(y por el paciente debidamente informado) como un gesto de prudencia más que como un fracaso técnico o personal. En caso de poca experiencia, se recomienda
seleccionar a pacientes con una patología
biliar no complicada.
Comparada con la técnica por laparotomía, la colecistectomía laparoscópica reduce el riesgo de complicaciones cardiopulmonares postoperatorias, pero no disminuye la respuesta
inmunitaria ni el traumatismo tisular, valorado por criterios
secundarios (interleucinas, proteína C reactiva
[PCR], adrenalina, cortisol) ni evita la
reacción catabólica postoperatoria.
Las ventajas de la colecistectomía laparoscópica sobre la realizada
mediante minilaparotomía se han demostrado en siete ensayos
terapéuticos según criterios clínicos. Para ser una técnica
considerada sin duda alguna «mejor», los resultados son menos evidentes
de lo que cabría esperar;
sobre todo cuando el bienestar postoperatorio (dolor y vómitos)
o la duración de la hospitalización se valoran con una técnica
«ciega».
Valoración quirúrgica preoperatoria
En función de los datos de la anamnesis y de la exploración clínica durante la entrevista anestésica preoperatoria, hay que solicitar
de forma selectiva
las pruebas que serán útiles para evaluar
el riesgo quirúrgico.
La ecografía hepatobiliar es el método de referencia para diagnosticar una colelitiasis. También ayuda en el diagnóstico de la colecistitis aguda. El momento óptimo para el tratamiento quirúrgico mediante laparotomía
se
sitúa en las
primeras 48 horas
de la colecistitis aguda.
El riesgo de fracaso de la laparoscopia y de conversión a una cirugía
por laparotomía aumenta
en función del tiempo que transcurre entre el
inicio de la colecistitis y la intervención. Si no se ha
realizado en semi-urgencias, parece preferible posponer la intervención 6-8 semanas. La ecografía hepatobiliar determina el número y el tamaño de los cálculos de la vesícula
y los calibres de los conductos
cístico y colédoco.
Si este último está dilatado, la detección de los cálculos
que se localizan
en él es más sencillo.
La solicitud de otras posibles
pruebas diagnósticas depende
de la forma en la que el cirujano
concibe el tratamiento de la coledocolitiasis.
La colangiografía peroperatoria durante la colecistectomía laparoscópica puede llegar a realizarse en más del 90 % de los casos. La capacidad
de tratar los cálculos diagnosticados mediante laparoscopia aumenta
la tasa de éxito.
La sensibilidad de la colangiografía peroperatoria bajo fluoroscopia para el diagnóstico de los cálculos
de la vía biliar principal
supera el 95 %. Se podría
evitar de forma selectiva
en los pacientes que tuvieran
un bajo riesgo de coledocolitiasis. La puntuación que permite realizar esta discriminación viene dada por: R = 0,04 x edad + 3.1 (si el calibre del colédoco
>10 mm en la ecografía) + 1,2 (si los cálculos de la vesícula
< 10 mm) + 1 (si hay cólicos
hepáticos) + 0,7 (si hay colecistitis aguda). La probabilidad de no tener cálculos en la vía biliar
principal (valor
predictivo negativo) supera
el 97 % cuando R <= 3,5. En un paciente con litiasis biliar sintomática, sólo la colangitis (dolor, fiebre, ictericia) y la ictericia preoperatorias se asocian a una probabilidad mayor del 50 % de Coledocolitiasis ( Neugebauer, 2000).
Las únicas indicaciones validadas para realizar una colangiografía retrógrada endoscópica (CRE) preoperatoria son la colangitis grave para el drenaje por esfinterotomía endoscópica (EE) urgente de la bilis infectada, y la
intención de tratar mediante
EE sin colecistectomía asociada una coledocolitiasis
en pacientes cuyos riesgos quirúrgicos
inmediatos sean considerados como demasiado grandes (puntuación
ASA 3).
La sensibilidad y la especificidad de la ecoendoscopia
para el diagnóstico de coledocolitiasis son del 92 y del 100 %, respectivamente. Comparada con la CRE y la colangiografía peroperatoria, la colangiografía por resonancia magnética (RM) tiene un 15 % de falsos
positivos y un 9 % de falsos
negativos.
Posición del
paciente y vía de abordaje
Organización del
quirófano normas generales
La laparoscopia aumenta la complejidad de la organización general del quirófano debido al estorbo de los aparatos necesarios. El cirujano debe asegurarse de que todo el personal que ayuda en la operación
esté preparado para este tipo de cirugía, conozca el
procedimiento y domine la técnica
de los diferentes dispositivos necesarios: cámara y fuente de luz, cable de transmisión de luz, monitor, aparato de insuflación y fuente de C02, aparato de electrocoagulación y dispositivo de irrigación- aspiración. La instalación de todos estos aparatos
conlleva un tiempo de ocupación
de los quirófanos que, a veces, se subestima.
La colocación del paciente
sobre la mesa del quirófano y de los diferentes
aparatos se hace en función
de las dimensiones de los mismos y de la movilidad
del fluoroscopio necesario
para la colangiografía peroperatoria.
La preparación del material necesario para la cirugía laparoscópica de la coledocolitiasis no es sistemática. Puede estar justificado realizar una valoración de la posible presencia de este cuadro en una fase preoperatoria por la información que se puede aportar al personal quirúrgico.
Material necesario
Equipo básico
La mesa es convencional, motorizada, y permite la traslación, el ascenso,
el descenso, las posiciones en declive y proclive y una lateralización que va de +20° a -20°. Permite un acceso radiológico y ofrece
la posibilidad de añadir diversos tipos de accesorios que puedan instalarse durante la cirugía:
apoyabrazos, férula
de Quénu, tope púbico,
apoyapiernas de Goepel,
cabezal y accesorios de protección y de seguridad (colchón y cojines
de gelatina).
El sistema de aspiración de vacío está controlado por un manómetro y se conecta a los bocales
mediante tubos. El generador de energía
suele ser un sistema
de electrocoagulación controlado mediante pedales
(monopolar y bipolar).
El electrodo neutro (placa) se pone sobre el muslo y está controlado con una alarma sonora de seguridad.
Material específico de
videocirugía
El material de videocirugía comprende una fuente de luz fría con dos tipos de bombilla:
una de xenón de 300 vatios (con una duración
de 500 horas) y una halógena (con una duración de 150 horas). La fuente de luz está conectada
a la cámara mediante un cable de fibra óptica que debe comprobarse de forma periódica
debido a su fragilidad. Su función es regular la intensidad de la luz que llega a la cámara.
El término cámara endoscópica engloba el captor
CCD, el cable de unión, la unidad de mando y el acoplador. El captor CCD de imagen de vídeo, también denominado cabeza
de la cámara, transforma
la imagen óptica en imagen de vídeo.
Existen dos tipos de cámaras:
la mono-CCD y la tri-CCD. Esta última recibe de forma separada
3 imágenes: una roja, una verde y una azul, y ofrece la resolución de color más fina.
Un cable
eléctrico multifilamento blindado garantiza la unión
entre la cabeza de la
cámara y su dispositivo de control.
Las cámaras convencionales ofrecen al cirujano una imagen ampliada
en dos dimensiones. Los estudios
comparativos no han demostrado ventajas significativas para los sistemas
de cámaras en tres dimensiones en el caso concreto de la
colecistectomía laparoscópica.
La pantalla de vídeo o monitor es el eslabón final de la cadena del sistema de endoscopia. Su papel es recomponer la imagen captada por la cámara. Para conseguir una buena calidad de visión, la
distancia entre el ojo y la pantalla
debe ser unas
tres a cinco veces la diagonal de la
pantalla del monitor.
Material para la colecistectomía
laparoscópica
El instrumental de laparoscopia es un material costoso y frágil
que comprende toda una gama de instrumentos de 5 mm y 10 mm de diámetro,
que deben desmontarse para que se puedan limpiar
y esterilizar.
Los instrumentos
necesarios para la colecistectomía laparoscópica son simples y poco numerosos:
-
dos trocares desechables o reutilizables, con un
diámetro de 5 mm y dos con un diámetro
de 10 mm;
-
dos pinzas de prensión atraumáticas y fenestradas, una de ellas debe ser hemostática
(0: 5 mm);
-
un gancho
de disección y electrocoagulación (0: 5 mm);
-
unas tijeras hemostáticas
(0: 5 mm);
-
una pinza de
colangiografía (0: 5 mm);
-
una pinza con clips reabsorbibles (0: 10 mm);
-
una cánula de irrigación-aspiración (0: 5 mm);
-
un disector
de 5 o 10 mm de diámetro;
-
una aguja de
punción (0: 5 mm);
-
un cable de conexión con la fuente
de electrocoagulación;
-
un tubo de conexión entre el insuflador y el trocar;
-
un cable de luz
fría;
-
un endoscopio rígido «óptico a 0°» (0: 10 mm).
Una parte del instrumental de laparotomía sirve tanto para colocar los trocares
como para extraer la vesícula.
Comprende:
-
un mango de bisturí;
-
un par de separadores de tipo Farabeuf;
-
una pinza de
disección atraumática
de tipo Backey;
-
una pinza de
disección con dientes;
-
dos pinzas con dientes de tipo Kocher;
-
un porta-agujas;
-
unas tijeras;
-
una pinza de
cálculos de tipo Mirizzi o Magil. El material
desechable estéril que se utiliza
es:
-
un estuche
de campos quirúrgicos para colocar al paciente con las
piernas en abducción;
-
un filtro bacteriano para el
insuflador;
-
una funda para la cámara
para evitar los inconvenientes de la esterilización sobre la cámara;
-
una funda para el
amplificador de intensidad luminosa;
-
un catéter de tipo intravenoso de calibre 17 G, una jeringa de 20 ml y un medio de contraste para la colangiografía;
-
una aguja de
neumoperitoneo de tipo Veress (si fuera necesario);
-
los tubos para conectar el
lavado-aspiración (suero salino
isotónico);
-
una bolsa para la extracción de la
vesícula.
Conversión
La probabilidad de convertir la operación
en una laparotomía por fallo o complicación de la técnica de laparoscopia oscila entre un 5 % y un 20 %, en función de la experiencia y las indicaciones quirúrgicas. Es más elevada cuando el paciente
es intervenido por una complicación aguda de la litiasis.
Esta decisión de convertir
la operación se toma a veces en una
situación de urgencia, debido
a una complicación hemorrágica peroperatoria. Como norma de seguridad, se debe disponer de forma sistemática en el quirófano de todo el material necesario para
realizar una laparotomía.
Fuente de
energía
El gancho de electrocoagulación monopolar fue inventado
para esta técnica. Se ha comentado
mucho sobre los riesgos
de las corrientes monopolares cerca de la vía biliar principal, y sobre los riesgos de difusión
de la corriente mediante
el fenómeno de arco eléctrico
o por la conducción a través de los clips metálicos. La disección puede hacerse con las tijeras y no con el gancho.
Se deben recordar
algunas normas
simples:
-
se debe revisar el aislamiento de la vaina en todos los instrumentos susceptibles de ser conectados a la fuente de electrocoagulación. Una parte no aislada puede crear un fenómeno de arco eléctrico, que es muy peligroso ya que puede producirse fuera del campo de visión;
-
la coagulación mediante pinza
bipolar evita los riesgos
de una coagulación accidental
fuera del campo visual. Sin embargo,
puede provocar corrientes de conducción si está cerca de clips metálicos, cuyo peligro es la
estenosis secundaria isquémica
del colédoco.
-
cualquier electrocoagulación hay que realizarla bajo control visual. El gancho coagulante se utiliza separándolo del colédoco
y no al revés;
-
el láser YAG no presenta ventajas con respecto a la electrocoagulación monopolar. El disector con ultrasonidos ha sido considerado, «de forma subjetiva», ventajoso para la disección
de elementos pediculares cuando están infiltrados por edema o grasa.
-
Anestesia y cuidados perioperatorios
La cirugía abdominal laparoscópica requiere anestesia general con intubación. La sonda nasogástrica se coloca bien de forma sistemática, bien siguiendo las indicaciones del cirujano
si observa que la cavidad gástrica
está dilatada y se retira al final de la intervención.
Las indicaciones de la
sonda vesical se reservan a las intervenciones que duran más de 120 minutos.
Una vez que se crea el neumoperitoneo ha de comenzarse la vigilancia continua de la proporción de gas carbónico
del aire espirado
mediante un capnógrafo.
El objetivo del neumoperitoneo es crear un espacio quirúrgico. El volumen obtenido
para una presión
determinada es función
de la relajación muscular de la pared. Mantener la normotermia no es algo prioritario para una colecistectomía laparoscópica cuya duración se prevé entre 45 y 75 minutos,
sin embargo la intervención puede prolongarse por la presencia de cálculos
en el conducto colédoco.
Estasis venosa y anticoagulación profiláctica
El decúbito prono y el incremento de la presión intraabdominal disminuyen el retorno
venoso de las extremidades inferiores y aumentan
la presión en las venas femorales.
Con relación a la activación de la coagulación sistémica después de la colecistectomía laparoscópica, las informaciones publicadas han sido contradictorias. Es posible que el obstáculo del retorno venoso de los miembros
inferiores, el incremento de la presión intraabdominal y la activación del sistema fibrinolítico aumenten el riesgo de trombosis venosa en este territorio durante la colecistectomía laparoscópica aunque no se ha establecido la incidencia real de las complicaciones tromboembólicas. Los efectos negativos relacionados con la posición
del paciente y el aumento de la presión intraabdominal pueden ser contrarrestados por los dispositivos de compresión venosa intermitente de los miembros inferiores. Por todas estas razones, parece prudente
que se proponga
una profilaxis de la trombosis
venosa a este nivel en todos los pacientes intervenidos de colecistectomía laparoscópica mediante heparina de bajo peso molecular
y medias elásticas que reduzcan la estasis
venosa.
Profilaxis del dolor postoperatorio
En estudios controlados y aleatorizados, se ha demostrado
que los siguientes métodos pueden reducir el dolor postoperatorio después de la colecistectomía
laparoscópica:
-
aspiración del gas residual al final de la operación;
-
instilación intraperitoneal
de suero;
-
instilación intraperitoneal
de anestésicos;
-
infiltración de los orificios
de los trocares con anestésicos locales.
Un estudio aleatorizado francés no confirmó la eficacia de la administración intraperitoneal de bupivacaína sobre el dolor postoperatorio tras colecistectomía laparoscópica;
-
la utilización de trocares
de 2-5 mm puede mejorar de forma secundaria el dolor postoperatorio y el resultado estético después de la
colecistectomía laparoscópica frente a los trocares
de 5
mm y 10 mm. La utilización de mandriles
con expansión radial puede reducir el dolor postoperatorio si se compara con los mandriles
cortantes.
Profilaxis antibiótica
En la laparotomía,
un metaanálisis recomendaba la profilaxis antibiótica. Esta
indicación sistemática ha sido puesta en duda por los resultados de dos estudios
aleatorizados sobre laparoscopia; la profilaxis antibiótica debe reservarse a los pacientes operados por una complicación aguda de la litiasis.
Profilaxis de las náuseas
y vómitos postoperatorios
Se estima que la incidencia de náuseas
y vómitos tras la
colecistectomía laparoscópica está entre el 10 y el 20 %. Varios estudios controlados aleatorizados han valorado la influencia de los fármacos
antieméticos (dimenhidrinato, ondansetrón, granisetrón, droperidol, metoclopramida, hioscina transdérmica) sobre la prevención y el tratamiento de las
náuseas y los vómitos.
Posición del paciente
El paciente se coloca en decúbito dorsal, con las piernas separadas, y en posición anti-Trendelenburg. El cirujano se sitúa entre las piernas del paciente
(posición denominada «francesa ») y el primer auxiliar
a la izquierda del paciente.
Si se considera necesario, un segundo
auxiliar se sitúa a la derecha del primero.
El sistema de vídeo se coloca a la derecha
de la cabecera del paciente.
La anestesia es general;
durante la intervención se mantiene una sonda nasogástrica, con el fin de evitar una punción accidental de estómago
distendido con la aguja de Veress que podría impedir
una buena visión del campo operatorio.
La colocación del paciente sobre la mesa de operaciones y las complicaciones que pueden
aparecer son responsabilidad del cirujano y del anestesista. Según la ley francesa
esta responsabilidad sólo implica al
equipo de enfermería
de anestesia
y de cirugía de forma delegada.
1 Posición del
equipo.
El paciente se coloca en decúbito supino. La cabeza descansa sobre un cabezal
de gelatina. Uno de sus miembros
superiores descansa
sobre un apoyabrazos relleno, fijo y en abducción inferior a 90°; el otro brazo se pone a lo largo del cuerpo, protegido en una férula de Quénu para permitir
el paso del amplificador de intensidad luminosa. Las extremidades inferiores se colocan
en abducción. Las piernas
se ponen en un apoyapiernas de Goepel con las rodillas flexionadas a 5°. Para evitar el deslizamiento
del paciente en la mesa de operaciones cuando se sitúa en proclive
se coloca un tope púbico.
El paciente se coloca en proclive a 10°-20° y rotado hacia la izquierda. La mesa se baja lo suficiente como para que el cirujano pueda operar con
los hombros completamente relajados y los codos flexionados a más
de 90°.
La columna de vídeo se instala
a la derecha del paciente, a la altura del hombro. Para
facilitar la visión, la distancia
entre el ojo del cirujano
y la pantalla debe ser unas
3-5 veces
la diagonal de la
pantalla del monitor.
La posición en «equipo doble» permite al cirujano colocarse entre las piernas abiertas del paciente. El primer ayudante se sitúa a la
izquierda del paciente y el instrumentista a su lado. Si fuera
necesario un segundo ayudante, éste se pondría
a la
derecha del paciente.
La colocación de otros aparatos tiene en cuenta la organización del quirófano
y de los enchufes, pero también la
ergonomía operatoria. Para crear el campo quirúrgico se utilizan paños
autoadhesivos no de tela. El campo expone todo el abdomen y debe adaptarse
a los trocares accesorios, a un posible
drenaje y a una posible conversión a un procedimiento de laparotomía.
Neumoperitoneo
Se suelen utilizar dos técnicas para
crear el neumoperitoneo. La primera, «cerrada», emplea la aguja de
Palmer o de Veress
que se introduce en la
cavidad abdominal para insuflar
gas y luego inserta a ciegas el primer trocar. La segunda, «abierta», fue descrita por Hasson y consiste
en introducir el primer trocar de forma «quirúrgica» bajo control visual y
a continuación comenzar
la insuflación.
Se calcula que la morbilidad asociada a la creación del neumoperitoneo y a la inserción
del primer trocar está por debajo
del 1 % de los casos, pero debido a múltiples sesgos, la incidencia real de lesiones viscerales y vasculares se sigue ignorando. Seis ensayos controlados aleatorizados han demostrado que la técnica «abierta» causa menos complicaciones, es más rápida y menos cara que la técnica
que utilizaba la aguja de Veress.
En un análisis global, las tasas de complicaciones eran del 2,8 % (16/574) con la técnica
«abierta» y del 11,6 % (64/552)
con la aguja de Veress.
En las auditorías prospectivas o retrospectivas, la incidencia de lesiones
viscerales y vasculares era respectivamente del 0,09 % en 265 737 pacientes
y del 0,096 % en 269 178 pacientes operados con una técnica
«ciega», y del 0,05 y 0 % en 14 614 pacientes
operados con una técnica
«abierta». La incidencia de embolia
gaseosa es inferior
al 0,6 %. Aparece en más del 60 % de los casos cuando se crea un neumoperitoneo y se perfora
un vaso de forma accidental con la aguja de Veress.
A pesar de estos datos, las sociedades científicas no han publicado
ninguna recomendación sobre la elección
de una u otra técnica hasta
la fecha.
Características del gas
En comparación con el CO2, la insuflación de la cavidad peritoneal con otros gases (helio,
N20, argón) no presenta
ventajas clínicas demostradas. El calentamiento y la humidificación del gas que se va a insuflar tienen efectos clínicos limitados y en un estudio
son contradictorios. El dolor postoperatorio que se irradia al hombro derecho o a los dos hombros se debe al estiramiento del diafragma
durante el neumoperitoneo. Una presión
de 5 a 7 mm Hg disminuye
el dolor postoperatorio frente a presiones
de 12 a 15 mm
Hg.
Suspensión parietal
La laparoscopia con suspensión parietal parece evitar los efectos secundarios del neumoperitoneo en los pacientes que tienen enfermedades asociadas (ASA III-IV).
En los pacientes
ASA I-II, la suspensión parietal conlleva menos alteraciones
hormonales, hemodinámicas y respiratorias, y mejora el
bienestar postoperatorio. Estos resultados no siempre
se han
confirmado. Aunque la exposición del campo quirúrgico es de peor calidad la suspensión parietal parece facilitar la operación
en caso de colecistitis crónica.
Exploraciones diagnósticas peroperatorias
Colangiografía
peroperatoria
La colangiografía mediante cateterismo del conducto cístico tiene unas tasas de éxito más elevadas
y permite una mejor visualización del árbol biliar que la colangiografía por punción
directa de la vesícula. La colangiografía bajo fluoroscopia permite una exploración en tiempo real de la vía biliar principal, la discriminación rápida entre las burbujas
de aire y los cálculos,
y disminuye los riesgos de falsos
positivos. La compresión suave del colédoco con un instrumento atraumático, bajo control
directo fluoroscópico, permite diferenciar una imagen de vacío relacionada con una burbuja de aire de una verdadera
imagen de cálculo,
y permite lograr la inyección
correcta del árbol biliar hepático
sin necesidad de recurrir
a ayudas farmacológicas (sulfato de morfina,
glucagón). La tasa de falsos positivos en estos casos es inferior
al 1 %. La colangiografía bajo fluoroscopia es más rápida que la realizada
con radiografías simples estáticas. La colangiografía peroperatoria permite un control
anatómico del árbol biliar
y, cuando no se realiza, se asocia a un retraso del diagnóstico y a un aumento
de la morbilidad de las lesiones
biliares. En los dos ensayos
que han valorado la colangiografía peroperatoria sistemática, la única lesión biliar grave descrita apareció en el grupo en el que no se realizó el procedimiento. Para que éste contribuya a la seguridad de la colecistectomía laparoscópica,
se deben respetar
ciertas reglas simples:
-
los elementos anatómicos que se han ido identificando durante la disección deben asegurarse con clips y
no seccionarse antes de la colangiografía;
-
la colangiografía debe permitir
el estudio de las vías biliares principales en su
conjunto: mapa intrahepático completo (identificar todos los conductos sectoriales), unión superior de los conductos hepáticos derecho e izquierdo,
unión inferior del cístico
y del conducto hepático común, colédoco terminal y pasos duodenales;
-
tras una colangiografía considerada normal, ningún conducto no identificado con anterioridad debe ser seccionado del lado del pedículo
hepático;
-
la búsqueda
de cálculos requiere radiografías
simples en cortes finos o un medio de contraste diluido, mientras
que la exploración anatómica
de los conductos intrahepáticos requiere
un contraste óptimo.
Ecografía
biliar peroperatoria laparoscópica
Los ecógrafos disponibles son aparatos multifrecuencia que permiten
la obtención de imágenes de resolución inferior al milímetro. La sonda de ecolaparoscopia se suele
introducir a través del trocar
umbilical de 10 mm de calibre,
y su progresión se sigue mediante
control visual. El extremo flexible de la sonda se coloca sobre la superficie de la cápsula hepática. La vesícula biliar se explora a través del segmento
V del hígado y la unión biliar superior a través del IV. La exploración del pedículo hepático se realiza antes que cualquier disección. Si se hacen movimientos de rotación
axial sobre la sonda que está colocada sobre la cara anteroextema del pedículo,
se pueden identificar las vías biliares principales y los elementos
vasculares del pedículo.
El modo doppler color facilita
la identificación de los elementos
vasculares.
Cuando se ha identificado la vía biliar, se sigue su trayecto
de arriba a abajo sobre la superficie lateral del
pedículo y se explora
su parte terminal
a través de la pared duodenal.
Los criterios de interpretación esenciales son el calibre
de la vía biliar y las
posibles imágenes hiperecógenas asociadas a un cono de sombra posterior que refleja la presencia
de cálculos en la misma. La ecografía
permite además
identificar determinadas anomalías de la anatomía biliar
pedicular. Varios estudios han valorado la ecografía
biliar peroperatoria bajo laparoscopia. De forma global, este procedimiento tenía más éxito que la
colangiografía peroperatoria, y se realizaba en menos tiempo y con una especificidad mayor para diagnosticar cálculos, aunque menor precisión a la hora de visualizar
la anatomía del árbol biliar. La sensibilidad era inferior o igual que la de la colangiografía. La ecografía biliar peroperatoria bajo laparoscopia depende del cirujano
que la realiza, es necesario aprender la técnica
(20-40 exploraciones) y no diagnostica las lesiones biliares.
Exploración e introducción de otros trocares
Una vez que se ha introducido la óptica se lleva a cabo una exploración global de la cavidad peritoneal para
comprobar que no hay adherencias
u otras
patologías no diagnosticadas.
A continuación se introducen los otros tres trocares
bajo control visual.
Su punto de inserción
es variable en función de la anatomía de paciente.
Se coloca un segundo
trocar de 5 mm a la altura del costado
derecho, lateralmente sobre la línea axilar anterior y más o menos bajo en función del borde inferior del hígado, con el fin de disponerlo lejos de la vesícula. Se introduce la pinza de prensión vesicular, fenestrada y atraumática. Se introduce un tercer trocar de 5 mm en posición infraxifoidea, a la izquierda o a la derecha del ligamento suspensorio. Se colocará un separador
hepático espatulado o una cánula de aspiración-irrigación. Asimismo, se introduce un cuarto
trocar de 10-11 mm, denominado «trocar quirúrgico», a la altura del costado izquierdo, por dentro de
la línea medioclavicular y a
una altura
variable en función
de la localización del
hígado y de la
VB.
Se introducirán los instrumentos de disección
(tijeras, electrocoagulación con gancho, disector, tampón montado, etc.) y la pinza con clips. Los trocares
n. o 2 y 4 deben disponerse de modo que los instrumentos quirúrgicos en el triángulo de Calot formen un ángulo de trabajo de 90 0 (principio llamado de «triangulación»). Una vez que los trocares estén en su sitio,
se controlará visualmente el punto de colocación
del primer trocar (introducido a ciegas)
para asegurarse de que no hay complicaciones asociadas con la introducción (hemorragia,
lesión visceral transfixiante, etc.).
Representación esquemática de la
posición de los trocares durante una colecistectomía laparoscópica. A. En condiciones
normales. b. En el
paciente obeso y en caso de una colecistitis difícil.
En casos complicados o en presencia
de un lóbulo hepático izquierdo que obstaculiza y se desborda
hacia la derecha,
a menudo es útil sujetar el ligamento redondo hepático mediante un punto transcutáneo (Nylon
2/0 con aguja derecha), situado a ambos lados del ligamento suspensorio y transfixiando el ligamento
redondo cerca de su inserción
hepática. Se tensan y anudan ambos extremos en el exterior. Esta maniobra eleva la cara inferior
del hígado y permite evitar, en la mayoría
de casos, tener que colocar un trocar
n. o 5 para mejorar la exposición. No obstante, si éste se considerara
necesario, debería situarse
a media distancia entre los trocares
n.
o 1 y 4.
Visión quirúrgica de la suspensión del
ligamento redondo
por un hilo transfixiante.
Disposición de
los trocares
El trocar óptico tiene un calibre de 10 mm y se sitúa en la zona umbilical. La
elección de una óptica
a 0 o 30° depende del cirujano. En un paciente
de corpulencia mayor de lo normal, una óptica a 30° puede tener más ventajas para la visualización de la región infrahepática si se ha optado por introducirlo por el ombligo. Si sólo se dispone de una óptica
a 0°, una alternativa consiste en desplazar hacia
arriba y hacia el hipocondrio derecho el
lugar de introducción del primer trocar.
Posición de
los trocares (A, B).
1. Trocar umbilical de 10 mm: trocar óptico. 2. Trocar epigástrico de 5 mm. 3. Trocar lateral derecho de 5 mm. Trocar del flanco
izquierdo de 10 mm:
trocar operador.
La óptica de la cámara se introduce por el trocar umbilical. Si sólo se dispone de un soporte automático de la cámara, el ayudante ha de sujetarla con la mano izquierda. La presión del dedo sobre el lugar elegido para cada uno de los otros trocares se valida con el control visual laparoscópico y se introducen también visualizándolos.
El trocar epigástrico tiene un calibre de 5 mm. Se suele localizar a la izquierda del ligamento redondo y del ligamento suspensorio del hígado. Hay que evitar lesionar estas estructuras durante la introducción. En este momento, hay que comprobar que el estómago no se ha dilatado con las maniobras de ventilación con la mascarilla. El trocar epigástrico se utiliza para introducir una pinza de prensión fenestrada y se confía a la mano derecha del ayudante. Si las circunstancias quirúrgicas lo justifican, este trocar permite la introducción de una cánula de irrigación-aspiración que puede servir para separar el hígado de forma simultánea.
El trocar lateral derecho tiene un calibre de 5 mm. Se introduce en función de la unión del ángulo derecho del colon. Se suele colocar un poco por delante de la línea axilar derecha, a una distancia suficiente de la región infrahepática para que las maniobras del cirujano no se vean entorpecidas por la longitud intraabdominal de la vaina del trocar. Este trocar sirve para introducir una pinza de prensión para la mano izquierda del cirujano. Para la disección del trípode coledococístico, el cirujano toma el infundíbulo de la vesícula, traccionando hacia abajo y hacia fuera. Esta maniobra abre el llamado triángulo de Calot. Todos los autores franceses consideran que la abertura de este ángulo coledococístico mediante las maniobras de exposición contribuye a aumentar la seguridad de la disección y previene el riesgo de lesiones biliares. Sin embargo, ningún estudio permite confirmar que este método «francés» de exposición se asocie a un menor riesgo de lesión biliar. Ese trocar también se emplea para introducir la pinza de colangiografía.
El trocar operador tiene un calibre de 10 mm, lo que sólo está justificado por la decisión de emplear clips reabsorbibles en cualquier cirugía biliar. Los demás instrumentos introducidos en ese trocar (gancho de electrocoagulación, disector, tijeras, cánula de aspiración) tienen un calibre de 5 mm. El cirujano elige un lugar de introducción a la izquierda de la línea media, de forma que el ángulo formado entre una pinza introducida por el trocar lateral derecho de un lado y el trocar operador del otro sea, al menos, de 90°. Si los orificios de los trocares están muy cerca los unos de los otros, o si los instrumentos trabajan formando un ángulo agudo, se crean unas condiciones quirúrgicas incómodas, es decir, inseguras. Cuando el trocar operador se haya introducido, se utiliza para conectar la insuflación del gas y así se evita la formación de vaho sobre la óptica.
Técnica quirúrgica
El principio de la técnica quirúrgica no difiere en función de si la intervención se lleva a cabo por laparotomía o por laparoscopia, y sólo son específicos la posición del paciente, la vía de abordaje y el instrumental empleado.
Reglas básicas en el transcurso de una colecistectomía
•Inicio de la disección en la unión infundíbulo Cística.
•Contacto permanente con la pared vesicular.
•Uso cauteloso de la coagulación monopolar.
•Esqueletización progresiva de la arteria y del conducto Cístico.
•Disección retrógrada hasta el cuerpo vesicular con colocación de clips.
•Colangiografía peroperatoria sistemática.
Exposición del pedículo hepático y liberación de las adherencias perivesiculares
Una buena exposición del pedículo hepático es esencial antes de iniciar cualquier disección quirúrgica. El pedículo hepático se expone en un plano constituido por un espacio superoinferior retrayendo hacia arriba la cara inferior del segmento IV y hacia abajo el bloque duodenopancreático. En la cirugía abierta se utiliza una válvula maleable para elevar el hígado y de la mano del primer auxiliar para descender la primera porción del duodeno.
Representación esquemática de la exposición del pedículo hepático mediante laparotomía.
En la cirugía laparoscópica se habrá recurrido, respectivamente, a un separador hepático introducido en el trocar epigástrico (trocar n. o 3) y a colocar al enfermo en posición de anti-Trendelenburg.
Visión quirúrgica de la exposición del pedículo hepático durante una colecistectomía laparoscópica.
Es importante tener un abordaje vertical y anterior del pedículo hepático. En los pacientes obesos puede emplearse una óptica de 30 grados o colocar el trocar óptico en posición elevada. Con frecuencia existen algunas adherencias en la vesícula y el epiplón o el ligamento hepatoduodenal; raramente se trata del colon transverso derecho o del duodeno. Estas adherencias se seccionan con tijeras a ras de la pared vesicular.
Exposición de la región infrahepática
El primer instrumento introducido en la cavidad abdominal es una pinza de prensión fenestrada que se inserta bajo control visual a través del trocar epigástrico. Con ella se agarra de forma firme el fondo de la vesícula desplazándolo hacia fuera y arriba, a la vez que se eleva el borde inferior del lóbulo derecho del hígado. El control de la misma lo realiza el ayudante con su mano derecha. En el trocar lateral derecho se introduce una pinza de prensión fenestrada, sujetándola la mano izquierda del cirujano. Con ella tracciona el infundíbulo de la vesícula hacia abajo y afuera. El gancho de disección, o las tijeras, se introducen por el trocar operador. Aparte de cualquier inflamación patológica, la rodilla superior del duodeno y el ángulo derecho del colon pueden estar unidos a la vesícula por un ligamento cistoduodenal o cístico-duodeno-cólico que se debe liberar en un primer tiempo para exponer la región infrahepática.
Exposición de la región infrahepática.
Exposición del triángulo de Calot
Sea cual sea la vía de abordaje. La exposición de la cara anterior del triángulo de Calot se consigue por medio de una tracción lateral y hacia la parte inferior del infundíbulo vesicular con la ayuda de una pinza fenestrada que se introduce en el trocar n. o 2. con el objetivo de dejar expuesto el triángulo de Calot Y de situar el CC en ángulo recto con la VBP.
Exposición del pedículo hepático durante una colecistectomía laparoscópica mediante tracción lateralmente y hacia abajo del infundíbulo vesicular por medio de una pinza atraumática.
Para exponer la cara posterior del triángulo el infundíbulo vesicular se basculará hacia arriba y hacia delante mediante la pinza atraumática, mientras que el separador se hace retroceder hacia el interior del pedículo hepático. Una tracción excesiva del infundíbulo vesicular expone a un arrancamiento traumático del CC y a una angulación peligrosa de la VBP. Cuando la vesícula se halla distendida a menudo es necesario puncionarla con la aguja de Veress con el fin de vaciar el contenido líquido y permitir la prensión. Se hará un cultivo de la bilis obtenida.
Exposición de la cara posterior del infundíbulo vesicular levantando la vesícula hacia arriba y retrayendo el pedículo hepático hacia la izquierda y hacia arriba.
A. Visión laparoscópica de la vesícula biliar. Ligamento colecistoduodenal (flecha). B. Cara posteroinferior del ligamento colecistoduodenal (flecha). Continuidad con el peritoneo vesicular (Línea de puntos)
Disección del triángulo de Calot
Se inicia en la unión entre el infundíbulo y el conducto cístico mediante la incisión de la hoja peritoneal anterior, y después de la posterior a algunos milímetros de la pared vesicular. Durante toda la disección se mantiene el contacto con la vesícula biliar. La unión infundibulocística debe visualizarse con claridad, permaneciendo lejos de la unión cisticocolédoco y evitando disecar la VBP.
Representación esquemática de la disección quirúrgica a distancia de la unión císticohepática coledocal.
Ligamento colecistoduodenal
A. Liberación de la hoja anterosuperior del ligamento colecistoduodenal.
B. Liberación de la hoja posteroinferior del ligamento colecistoduodenal. La línea de puntos marca la apertura del peritoneo.
Visión quirúrgica de la disección quirúrgica con gancho coagulador de la unión cístico- infundibular. Cara posterior.
El instrumento de elección continúa siendo el electrocoagulador aunque, en función de la preferencia del cirujano y de las dificultades, pueden utilizarse una pinza de disección o un tampón montado. La ventaja del gancho reside en aislar cada estructura anatómica menor atravesando el triángulo y seccionarlas después de la identificación y de la electrocoagulación.
Sin embargo, la coagulación monopolar debe emplearse con gran cautela (potencia débil y tiempo de coagulación corto) con el fin de evitar cualquier lesión térmica del pedículo hepático. La disección del pedículo cístico se pretende conseguir de manera retrógrada, esqueletizando progresivamente y con prudencia, sin seccionar la arteria y el conducto cístico.
Disección del pedículo cístico con gancho coagulador. a. Inicio de la disección. b. Fin de la disección.
El CC se aísla en una longitud de 10 mm a partir de la unión infundibulocística. No es preciso disecarlo más en la dirección de la VBP salvo en caso de empedramiento cístico. En ese caso, tras la abertura lateral del Ce. Se extraen todos los cálculos endocísticos.
La disección se lleva a cabo de manera retrógrada en la cara anterior y posterior del infundíbulo vesicular, entre éste y la cara inferior del hígado, donde puede existir una anomalía biliar como una convergencia biliar escalonada del canal posterolateral derecho.
Seguimiento retrógrado de la disección sobre el infundíbulo vesicular. En su cara posterior.
Convergencia biliar escalonada en el transcurso de una colecistectomía laparoscópica. a. Visión quirúrgica del canal posterolateral (cpld), del conducto cístico (ce), de la vía biliar principal (VB?) y de la rama derecha de la arteria hepática (Ram Der AH). b. Colangiografía peroperatoria que pone de manifiesto la integridad del canal posterolateral.
Esta disección se realiza permaneciendo a ras de la vesícula biliar y de manera atraumática. En esta fase, se libera por completo el triángulo de Calot, tanto en su cara ventral como dorsal. Y la vesícula biliar sólo queda unida por el fondo al lecho vesicular; es la técnica denominada de «bandera», descrita por Jean Mouiel, 1991.
Visión quirúrgica de la disección completa del triángulo de Calot en el transcurso de una colecistectomía laparoscópica.
Posteriormente se pinzan la arteria y el conducto cístico con la ayuda de clips de titanio (en caso de confusión con la VBP. este tipo de clip puede retirarse fácilmente, a diferencia de los clips reabsorbibles cerrados) Y no se secciona ninguna estructura canalicular dentro del triángulo de Calot antes de llevar a cabo una colangiografía peroperatoria (COP) que permite confirmar la integridad del árbol biliar extrahepático.
Visión quirúrgica de la disección completa del triángulo de Calot durante una colecistectomía laparoscópica con pinzamiento de dos ramas arteriales císticas y del conducto cístico antes de llevar a cabo la colangiografía peroperatoria.
Colangiografía peroperatoria
Por consiguiente la CPO se lleva a cabo tras una disección completa del triángulo de Calot y del infundíbulo vesicular por vía retrógrada.
Colangiografía peroperatoria, que debe efectuarse al final de la disección completa del triángulo de Calot
En estas condiciones la realización de una CPO va a permitir si se interpreta correctamente, diagnosticar un posible traumatismo quirúrgico de la VBP en más del 90% de los casos lo que conduce a una reparación biliar primaria en condiciones óptimas. Existen otros argumentos a favor de una CPO sistemática durante una colecistectomía laparoscópica:
- Disminución de la incidencia de traumatismos quirúrgicos de la VBP.
- Reducción de la gravedad de los traumatismos quirúrgicos de la VBP en caso de confusión entre el CC y VBP (en aproximadamente el 40% de los traumatismos biliares).
- Detección de anomalías anatómicas biliares (implantación canalicular anómala. canal de Luschka, etc.).
- Detección de litiasis no detectada de la VBP (Flum, 2003).
Desde el punto de vista técnico tras colocar un clip de titanio al lado de la vesícula se efectúa una incisión parcial del CC en su mitad anterior. Una vez que se ha seguido retrógradamente el CC para extraer una posible litiasis cística (se sospecha si no existe un buen reflujo de bilis a partir de la VBP).
El catéter de CPO se introduce varios milímitros en el CC; éste se ha purgado previamente con suero fisiológico asegurándose de que no haya rastro de burbujas en el sistema canalicular. El extremo del catéter se mantiene colocado en el CC gracias a un clip dispuesto con cuidado y apenas ceñido alrededor del CC o mediante una pinza de cpo adaptada.
Visión quirúrgica de la introducción del catéter de colangiografía peroperatoria por vía transcística.
Visión quirúrgica de la oclusión del catéter de colangiografía peroperatoria a nivel del conducto cístico. a. Mediante un clip de titanio. b. Por medio de una pinza de colangiografía de Olsen- Reddick.
Colangiografía.
A. Colangiografía con la pinza de Olsen.
B. Colangiografía con catéter transparietal.
La CPO se llevará a cabo por fluoroscopia dinámica, obteniéndose imágenes secuenciales a presión baja de la VBP baja y del paso duodenal y al final de la inyección, del árbol biliar extra e intrahepático complejo, en particular del lado derecho.
Tras efectuar la CPO, se retira el catéter y se cierra el muñón del CC con los clips de titanio, evitando lesionar la VBP y visualizando bien su ubicación. La arteria cística se secciona preferentemente antes del CC con el fin de evitar lesionarla accidentalmente.
Visión quirúrgica del cierre por clips del conducto cístico al final de la colecistectomía laparoscópica.
Colecistectomía propiamente dicha
La disección del lecho de la vesícula se realiza de forma retrógrada, es decir, desde el cuello vesicular hacia el fondo.
Las hojas de la serosa vesicular se cortan con el gancho coagulador o las tijeras. La sección del peritoneo se tiene que hacer manteniendo una distancia con el hígado. El plano «bueno» de disección es el que más se acerca a la vesícula. Cuanto más lejos de él, más cerca se está de la placa vesicular y mayor es el riesgo de despegarla del hígado. Este plano es más hemorrágico. El contra-apoyo que ejerce el ayudante al levantar el lecho vesicular hacia arriba facilita el despegamiento y la disección de la vesícula. Para ello, puede desplazar la pinza o el aspirador apoyado en el lecho vesicular o coger con la pinza el borde del peritoneo que se ha dejado del lado hepático. Durante esta disección, se recomienda poner un clip a los pequeños conductillos que se vayan encontrando, ya que puede tratarse de conductillos biliares accesorios que drenan directamente a la vesícula. Hay que recordar que todo este tiempo quirúrgico sigue a una colangiografía que ha permitido identificar la cartografía sectorial de los conductos biliares del hígado derecho, y localizar posibles anomalías o variaciones «peligrosas», como la duplicación del conducto derecho en sus componentes sectoriales o el deslizamiento hacia abajo del conducto paramediano o del conducto lateral derecho que pueden confluir con el conducto hepático muy cerca del conducto cístico.
Una variación bastante peligrosa es la unión de un conducto cístico corto directamente con el conducto lateral derecho. Cuando se ha liberado completamente la vesícula, se introduce en una bolsa de plástico que facilitará la extracción sin riesgo de fuga. La vesícula dentro de su bolsa se coloca de forma temporal en el espacio interhepatodiafragmático derecho. Aunque la intervención se haya desarrollado en condiciones ideales, siempre resulta útil en este momento comprobar la ausencia de cualquier derrame sospechoso, sobre todo biliar, y la calidad de los clips colocados sobre la arteria y el conducto císticos. Cualquier hemorragia que se detecte durante esta comprobación debe controlarse mediante una electrocoagulación lo más selectiva posible.
Las técnicas de coagulación «en sábana» del lecho vesicular son tan eficaces como peligrosas. Esta comprobación debe realizarse antes de la extracción de la vesícula, ya que en este estadio todavía se dispone de un buen neumoperitoneo. El control al final de la intervención permite acabarla sin drenaje aspirativo infrahepático.
Visión quirúrgica de la disección retrógrada del lecho vascular.
Si no hay restos inflamatorios importantes, el plano de disección entre el hígado y la VB es fácil de localizar y de disecar. En caso de identificar un canal de Luschka, éste se pinza selectivamente. Una vez que la VB se ha desprendido por completo, se sitúa en posición de espera encima del hígado con el fin de comprobar la hemostasia del lecho vascular.
Visión quirúrgica del lecho vascular al final de una colecistectomía laparoscópica.
Recuperación de la vesícula
La extracción de la vesícula en una bolsa de plástico facilita la maniobra, reduce el riesgo de contaminación parietal y tiene en cuenta la posibilidad, poco frecuente, de que exista un cáncer inadvertido de la vesícula.
Extracción de la vesícula en una bolsa facilitada al retirar los cálculos.
Clásicamente, el ombligo era el orificio elegido para la extracción de la vesícula. Esta elección respondía ante todo a una cuestión estética. En la práctica, el orificio umbilical está sujeto a infecciones y la fragilidad relativa de su cierre en un plano aponeurótico tiene riesgo de más complicaciones a medida que se va agrandando. Una alternativa consiste en elegir el orificio del trocar «operador», cuya ventaja es que se puede cerrar en dos planos aponeuróticos. La vesícula se extrae con la bolsa de protección con la precaución de coger el borde de la misma a la vez que el muñón cístico, lo que permite orientar bien la vesícula en su trayecto parietal. La bolsa se retira simultáneamente con el trocar. Una pinza fuerte tipo Kocher o Kelly asegura que se agarre el borde de la bolsa una vez fuera, lo que evita que se vuelva a introducir de forma intempestiva. La bolsa sirve como protección de la pared durante la maniobra de extracción y no para la propia extracción, dada su relativa fragilidad. La vesícula y los cálculos que contiene se extraerán en el interior de la misma mediante una tracción suave, con una dilatación si fuera necesario del orifico aponeurótico, una punción o una aspiración del contenido biliar de la vesícula, o mediante la extracción con o sin fragmentación mediante la pinza de cálculos en el interior de la vesícula. Es más seguro si se mantiene un control laparoscópico antes de extraer la bolsa de forma definitiva.
Visión quirúrgica de la extracción de la vesícula biliar por uno de los orificios de trocar de 10 mm.
a. Visión intraperitoneal después de aspirar la bilis intravesicular.
b. Visión externa de la extracción vesicular.
Desde el momento que el infundíbulo vesicular aparece en la superficie de la piel se sujeta mediante una pinza de Kocher. La vesícula se abre y después se vacía la bilis mediante aspiración con la jeringuilla después de una punción o por una cánula de aspiración.
Si los cálculos constituyen todavía un obstáculo en la salida de la vesícula, se extraen uno a uno o se fragmentan instrumentalmente. Si la pared vesicular es frágil, está inflamada y/o los cálculos son muy numerosos, deberá extraerse la VB dentro de una bolsa de plástico o de un guante quirúrgico con el fin de evitar cualquier contaminación parietal o diseminación litiásica intraperitoneal.
Visión quirúrgica de la vesícula biliar colocada dentro de un saco de extracción.
Verificación final y cierre
La intervención finaliza con una última inspección del campo quirúrgico, para detectar una posible hemorragia activa, una fuga de bilis o complicaciones en el lugar donde se introducen los trocares. El drenaje del lecho vesicular se efectúa a través de 17 un drenaje siliconado multiperforado, de 12 a 15 Fr, introducido por el trocar de 5 mm del lado derecho.
Colocación de un drenaje Silastic dentro del hiato de Winslow al final de la colecistectomía laparoscópica.
En los casos sencillos es opcional y en todos los casos de disección difícil o de colecistitis aguda se aconseja encarecidamente. Este drenaje tiene como objetivo evitar la formación de una colección subhepática, especialmente de un biloma en caso de fuga biliar a partir de un canal de Luschka o de un muñón cístico. Los trocares se retiran uno a uno comprobando que no hay hemorragia en su trayecto parietal. El abdomen se desinfla por completo después de retraer la óptica y se cierran los orificios cutáneos.
El cierre aponeurótico de los orificios de trocar de 10 mm o más se efectúa sistemáticamente para evitar una eventración postoperatoria. Finalmente, se inspecciona la pieza quirúrgica para detectar una posible neoplasia subyacente.
Cualquier fiebre, dolor o, de forma general, signo patológico en este intervalo no debe subestimarse, sino que debe poner en marcha de forma inmediata estudios que detecten precozmente una posible complicación: ecografía o tomografía computadorizada abdominal ante cualquier sospecha.
La misma noche de la cirugía, o al día siguiente, pueden pautarse bebidas y una alimentación ligera. El alta puede proponerse para la tarde del día siguiente de la intervención. La colecistectomía laparoscópica en cirugía ambulatoria no está prevista en la «cultura» de los pacientes franceses.
Variantes de la técnica «americana»
La técnica que se denomina «americana» se distingue de la «francesa» por la posición del paciente y de los cirujanos. Un estudio aleatorizado ha comparado estos dos métodos. De forma inesperada, los autores han concluido a favor de la técnica «francesa» por la menor repercusión que ésta tiene sobre la función respiratoria postoperatoria 1891. El paciente se coloca en decúbito supino con las piernas juntas. El cirujano se pone a su izquierda y el primer ayudante a la derecha. Un segundo ayudante que sujeta la cámara se coloca a la izquierda del cirujano. La columna de vídeo se pone a la altura del hombro derecho del paciente, que tiene el brazo derecho en abducción. El trocar óptico está en posición umbilical y permite el paso de una óptica de 10 mm a 45°. El paciente se pone en posición anti-Trendelenburg, girado hacia la izquierda de forma que «eleve» el hipocondrio derecho y separe las vísceras abdominales. Los otros tres trocares se insertan bajo control visual. El segundo trocar se coloca en posición epigástrica, a la izquierda de la línea media. Mide 10 mm para que puedan pasar la pinza de clips de 10 mm y la óptica al final de la intervención para comprobar que no existe hemorragia en el orificio umbilical.
Para elevar el ligamento redondo y el lóbulo izquierdo del hígado se introduce un instrumento por este trocar epigástrico y se sitúa a 90° con respecto al eje de la vía biliar principal.
Los dos últimos trocares tienen un calibre de 5 mm, uno está situado en la línea axilar derecha y el otro en el hipocondrio derecho, a lo largo del reborde costal, sobre la línea medioclavicular derecha, en la perpendicular de la unión entre el conducto cístico y el colédoco. Se empleará para la colangiografía peroperatoria. La pinza utilizada para coger el fondo de la vesícula se introduce por el trocar lateral derecho y empuja el fondo de la vesícula hacia arriba y la derecha, a la vez que eleva la cara inferior del lóbulo derecho. Una segunda pinza se introduce por el trocar medioclavicular y toma el infundíbulo de la vesícula que es empujado hacia abajo y la derecha, en dirección a la fosa ilíaca derecha. La finalidad de esta maniobra es aumentar la distancia entre el conducto cístico y el conducto hepático común, al abrir el triángulo de Calot. En un paciente no obeso, en este punto es posible identificar bajo el peritoneo la arteria cística, el ganglio de Mascagni, el conducto cístico y el colédoco. La disección comienza en la unión entre el infundíbulo y el conducto cístico con un instrumento introducido por el trocar epigástrico. Se realiza una incisión por delante en el peritoneo, a unos milímetros de la reflexión sobre el hígado del peritoneo vesicular en la zona media del cuerpo de la vesícula. Después se continúa hacia la unión vesiculocística. Se realiza la misma maniobra sobre la cara posterior de la vesícula, tras haber desplazado ésta hacia arriba y a la izquierda. El infundíbulo se separa del lado hepático trabajando de forma alternativa hacia delante y hacia atrás, hasta que pueda pasar un instrumento por detrás de la arteria y conducto císticos. Posteriormente, un disector separa estos dos elementos. El conducto cístico se diseca a partir del infundíbulo hasta su unión con el colédoco. Después de haber identificado la arteria y el conducto císticos, se introduce la pinza de clips por el trocar epigástrico. Se colocan clips tanto en la arteria como en el conducto cerca del infundíbulo y se abre éste por la cara anterior para realizar la colangiografía.
Colecistectomías difíciles
Las dificultades que se encuentran durante una colecistectomía laparoscópica se deben a una enfermedad biliar (colecistitis aguda, fístula biliodigestiva, pancreatitis aguda) o al paciente (variaciones anatómicas del pedículo, antecedentes de cirugía abdominal, obesidad, embarazo).
Colecistitis aguda litiásica
El riesgo de conversión en laparotomía para una colecistitis aguda litiásica alcanza el 15-20 %. Las dificultades pueden derivarse de una mala organización del tratamiento del paciente. El momento óptimo para el tratamiento quirúrgico de la colecistitis aguda es la intervención semi-urgente durante las primeras 48 horas de la enfermedad.
El riesgo de fracaso de la laparoscopia y de conversión en laparotomía aumenta a medida que crece el intervalo de tiempo entre el comienzo de la colecistitis y la operación. Si no se realiza en semi- urgencias, parece preferible retrasarla de 6 a 8 semanas, si es posible.
Para tratar la colecistitis aguda se deben conocer algunas particularidades técnicas de la colecistectomía laparoscópica.
- La infección aguda de la vesícula conlleva alteraciones inflamatorias de la región infrahepática. La exploración puede detectar la presencia de un derrame perihepático y adherencias epiploicas que oculten toda o parte de la vesícula.
Estos datos exploratorios, si no se está demasiado familiarizado con la técnica laparoscópica, deben hacer plantearse de forma razonable y rápida la conversión. A la inversa, si el paciente se interviene pronto, puede sorprender lo fácil que resulta separar estas adherencias de la vesícula, normalmente incluso con el aspirador, lo que va a permitir separar la «bolsa» epiploica de la vesícula tensa por la retención biliar infectada.
- En el caso particular del hidrocolecisto o de la colecistitis aguda, la presión de la pared vesicular no permite tomar la vesícula sin haber evacuado con antelación una parte del contenido por punción. Incluso después de ésta, a veces hay que separar y elevar la vesícula con la cánula de aspiración sin intentar coger la pared con la pinza.
- Se aplica sobre todo la norma de acceder primero al peritoneo situado por detrás del infundíbulo con el fin de «soltar » lo antes posible la vesícula de sus inserciones infrahepáticas.
Se trata de abrir un triángulo en el cual se podrá individualizar la arteria y el conducto císticos. No siempre es fácil encontrar un buen plano de separación. Por el contrario, una vez se identifica este plano, la separación de la vesícula resulta relativamente fácil y rápida por el edema asociado a la infección.
- En caso de colecistitis aguda, una tracción intempestiva y excesiva sobre la vesícula conlleva un despegamiento de la placa vesicular y este error de disección se acompaña inmediatamente de una supuración hemorrágica negruzca en sábana que, sin ser grave, dificulta la intervención.
- Las dificultades encontradas durante la disección en la colecistitis aguda hacen necesario comprobar la ausencia de lesión biliar mediante una colangiografía peroperatoria.
La colecistitis aguda se asocia a mayor riesgo de coledocolitiasis.
- La distensión del infundíbulo por encima del cálculo bloqueado en el conducto cístico provoca lo que se conoce como síndrome de Mirizzi, con compresión del pedículo hepático por esa distensión infundibular. Desde el punto de vista técnico, hay que saber que éste va a alojarse por detrás del pedículo y que habrá que «desenclavarlo» de esta localización sin lesionar los elementos más anteriores. Existe un riesgo de lesión, incluso de pérdida de sustancia, de la cara posterior de la vía biliar principal. En caso de arteria cística corta (cf. supra), las alteraciones inflamatorias pueden atraer un sifón de arteria hepática derecha que se pone en contacto o incluso se adhiere al infundíbulo. Si se desencadena una intensa hemorragia, se recomienda aplicar una pinza de prensión para garantizar la hemostasia transitoria y realizar una conversión rápida a laparotomía, antes que intentar maniobras de hemostasia peligrosas para el pedículo hepático derecho.
- Un error de identificación del plano de separación puede conllevar a la rotura de la vesícula si la pared está necrótica.
Esta abertura de la vesícula no es un accidente grave en sí. Obliga a realizar un buen lavado infrahepático y a recuperar todos los cálculos que puedan haber salido a la cavidad peritoneal. La bolsa de plástico que se utilizará para la extracción de la vesícula se introduce en el abdomen para poner dentro los cálculos, antes incluso de meter la vesícula. El hecho de que la vesícula se abra puede facilitar, de forma paradójica, la disección.
- El conducto cístico puede estar dilatado, destruido total o parcialmente por la erosión del cálculo bloqueado, o roto por las maniobras de disección. La colangiografía permite valorar la longitud de conducto disponible para una nueva disección más próxima de la confluencia con el conducto hepático. Si el calibre lo permite, el cierre del cístico requerirá dos clips reabsorbibles o una sutura intracorpórea mediante un hilo trenzado reabsorbible 00. La disección puede haber roto el cístico, en cuyo caso la identificación del muñón en los tejidos pediculares inflamados e infiltrados se convierte en un proceso azaroso. Un lavado de la región asociado a «masajes» del pedículo mediante la cánula puede ayudar a localizar una salida de bilis e identificar así el muñón cístico. Si no se consigue, no se puede aceptar la solución de no cerrar el cístico y dejar un drenaje aspirativo de contacto. Hay que convertir el procedimiento en laparotomía para continuar la disección en mejores condiciones, y si es necesario, con una ayuda adicional.
- La extracción de una vesícula cuya pared está alterada por la infección requiere realizar de entrada una incisión cutánea y aponeurótica suficiente. Resulta inútil intentar ganar 1 o 2 cm con una incisión parietal.
- Muchos cirujanos utilizan un drenaje aspirativo infrahepático en caso de colecistitis aguda aunque su utilidad no se ha demostrado. Si se retira el tubo de drenaje en las primeras 24 horas del postoperatorio no aumenta la morbilidad.
-
Colecistitis aguda o escleroatrófica mayor
La colecistitis aguda o escleroatrófica se asocia con un determinado número de dificultades quirúrgicas adicionales, relacionadas con procesos inflamatorios o fibróticos locales, lo cual supone tomar ciertas precauciones especiales en todas las fases de la disección quirúrgica.
Puntos clave en caso de colecistitis aguda o Colecistectomía en los 4 días siguientes al inicio del episodio agudo.
o Descompresión mediante punción de la vesícula con aguja de Veress. o Suspensión del ligamento redondo y/o el trocar n. O 5, si es necesario.
o Casos difíciles (Calot indisecable): vía anterógrada y/o endovesicular (v. apartado "Colecistectomía subtotal,).
o Saco de extracción sistemático (aumento de tamaño del orificio de extracción).
Colecistitis aguda diferida
Varios estudios retrospectivos o aleatorios (Navez, 2001. Kiviluoto, 1998) han demostrado que una intervención laparoscópica precoz (en los 4 días siguientes al inicio del episodio agudo) se asocia con una tasa menor de conversiones en laparotomía y de complicaciones postoperatorias, en comparación con una cirugía diferida después de un tratamiento médico con antibióticos. Cuanto más pronto se interviene quirúrgicamente la colecistitis aguda en la evolución del proceso inflamatorio, más se facilita la disección debido al edema. En caso de poca experiencia del cirujano se requiere con frecuencia la conversión a una laparotomía, como sucede en caso de colecistitis gangrenosa, incluso para un cirujano experimentado. Un factor notable de dificultades quirúrgicas independientemente de la demora es la presencia de residuos fibrosos perivasculares derivados de otros brotes inflamatorios agudos anteriores.
Exposición de la vesícula biliar
Con frecuencia, la vesícula se halla incluida dentro del plastrón inflamatorio perivesicular, que se desprenderá con un electrocoagulador, con un tampón o mediante la cánula de aspiración, separando el colon transverso derecho y el duodeno en las inmediaciones del infundíbulo. Las paredes inflamatorias y gruesas de la VB en la colecistitis aguda hacen difícil asirla. Por consiguiente, se aconseja puncionarla con la aguja de Veress al principio de la intervención quirúrgica y aspirar la bilis alterada o purulenta. Finalmente, las dificultades de exposición suelen obligar a colocar otro trocar adicional.
Disección del triángulo de Calot
La disección del triángulo de Calot implica especialmente un riesgo en las formas avanzadas de colecistitis aguda o de colecistitis escleroatrófica, en las que la VB es pequeña, se encuentra retraída sobre los cálculos, tiene paredes gruesas y una fibrosis retráctil significativa en el triángulo de Calot. Esta disección se efectuará con tampón montado sobre pinza atraumática o con un electrocoagulador, minimizando el uso de la coagulación monopolar.
Visión quirúrgica de la disección del pedículo hepático con tampón montado tipo peanuts sobre pinza atraumática en el curso de una colecistectomía laparoscópica para una colecistitis aguda.
La hemorragia es difusa, nubla el campo quirúrgico y obliga a irrigar y aspirar de manera permanente. La disección debe permanecer en contacto con la pared vesicular.
En determinados casos difíciles puede considerarse útil una vía anterógrada parcial que parte del fundus vesicular en dirección al triángulo de Calot, con la condición de permanecer estrictamente en contacto con el borde superior de la VB y de no seguir la disección en la dirección del pedículo hepático desde el momento que se han desprendido el fundus y el cuerpo de la vesícula.
Representación esquemática de una colecistectomía difícil en estados inflamatorios graves: disección vesicular anterógrada parcial, limitada en el fondo y en el cuerpo de la vesícula, detenida a nivel del infundíbulo vesicular y asociada con una abertura del cuello vesicular para desenclavar una macrolitiasis infundibular enclavada.
Si existe un macrocálculo enclavado en el infundíbulo vesicular que impide el acceso al triángulo de Calot, puede ser necesario abrir el infundíbulo (prestando atención a la hemostasia de la pared vesicular si la arteria cística no se ha controlado de antemano) y desenclavar el macrocálculo con la pinza; éste se coloca entonces en un saco de extracción situado en la cara superior de la parte derecha del hígado.
Visión quirúrgica de la abertura del cuello vesicular para desenclavar una macrolitiasis infundibular enclavada.
Esta técnica de abertura del infundíbulo es igualmente útil si la disección en el triángulo de Calot es peligrosa. Esta vía endovesicular permite controlar la disección de la pared vesicular desde el exterior y el interior, lo que mejora el reconocimiento de los límites de la VB en el triángulo de Calot, que presenta procesos inflamatorios significativos.
Tras la abertura voluntaria del infundíbulo vesicular, visión quirúrgica del control de la disección de la pared vesicular desde el exterior y desde el interior.
También es posible localizar el CC desde el interior y cateterizarlo para llevar a cabo la CPO.
En caso de inflamación aguda o escleroatrófica significativa que impide la disección del triángulo de Calot, de compresión de la VBP por el infundíbulo vesicular o, por último, en caso de convergencia biliar escalonada, puede considerarse útil llevar a cabo una colecistectomía subtotal, dejando una parte del infundíbulo vesicular para proteger el árbol biliar extrahepático (conducto hepático común o convergencia biliar escalonada)
Colangio-RM preoperatoria que pone de manifiesto varios factores de riesgo en un paciente intervenido quirúrgicamente por una colecistitis aguda enfriada: una macrolitiasis infundibular enclavada y un conducto cístico corto que nace de una convergencia biliar escalonada.
Colecistectomía subtotal, dejando en su sitio un patch de infundíbulo vesicular en los estados inflamatorios graves en que existe peligro en la disección del infundíbulo vesicular (compresión biliar, síndrome de Mirizzi, convergencia biliar escalonada, etc.). a. Representación esquemática. b. Visión quirúrgica.
En este caso, tras una CPO de control para asegurar la integridad del árbol biliar y que no existe ninguna litiasis en el colédoco asociada, se sutura selectivamente el CC por vía endovascular, se elimina con argón o electrocoagulación la mucosa del patch infundibular y se coloca un drenaje subhepático en el hiato de Winslow. Esta técnica resulta muy segura en las situaciones complejas. No obstante, conviene evitar que se diseminen los cálculos intravesiculares, lo cual puede ser molesto en caso de empedramiento múltiple. Asimismo, debe excluirse una neoplasia vesicular subyacente. En determinadas colangitis necróticas el plano de disección del lecho vascular es difícil de localizar o es inexistente. No es excepcional tener que dejar un fragmento de pared vesicular en el lecho vesicular para evitar dañar el parénquima hepático, lo que provoca una hemorragia abundante.
Colecistectomía subtotal: colangiografía peroperatoria por vía endovesicular.
Colecistectomía subtotal: sutura del conducto cístico por vía endovesicular.
Colecistectomía subtotal: vaporización con argón de la mucosa del patch infundibular que queda en su sitio.
Fístulas colecistoentéricas y biliobiliares
Las fístulas bilioentéricas son colecistoduodenales más que colecistocólicas. Deben considerarse, al margen de un caso particular de la cirugía biliar laparoscópica, como contraindicaciones para proseguir con la intervención laparoscópica. Si el trayecto fistuloso se puede individualizar de forma clara, la sección de la fístula en su vertiente digestiva (no vesicular) puede hacerse gracias a la aplicación de una (o dos) sutura-sección mecánica lineal, que se completará con puntos sueltos o una sutura interna. La continuación de la intervención biliar no presenta particularidades, excepto por la frecuencia de coledocolitiasis.
Las fístulas biliobiliares son cístico o infundibulohepáticas. Se observan en pacientes con enfermedad biliar aguda o tras varios brotes infecciosos tratados con fármacos. La imposibilidad de disecar bien el triángulo coledococístico suele conllevar la conversión en laparotomía que se deberá realizar como norma cuando se observan las fístulas en el laparoscopio.
Pancreatitis aguda
El tratamiento laparoscópico es posible en pacientes cuya litiasis biliar se haya diagnosticado junto con una pancreatitis aguda. La puntuación de Ranson evalúa la gravedad de la pancreatitis aguda. En las benignas, es inútil retrasar la cirugía por laparotomía más allá del intervalo necesario para el estudio del pronóstico de la enfermedad. En las formas graves, la cirugía de urgencias aumenta la morbilidad y se debe dar prioridad al tratamiento de la pancreatitis y de sus complicaciones. Además, durante la laparoscopia, la gravedad de la pancreatitis se asocia con mayores dificultades y a un mayor riesgo de conversión en laparotomía.
La tomografía computadorizada (TC) pancreática, realizada antes de la intervención biliar, valora el volumen de la glándula o de los seudo quistes necróticos, que pueden disminuir el volumen disponible para la intervención a la hora de crear el neumoperitoneo.
Anatomía del pedículo
Es necesario conocer la anatomía biliar para interpretar la colangiografía peroperatoria. Las variaciones de la anatomía de los conductos biliares aparecen sobre todo en los del lado derecho: subdivisión del conducto hepático derecho en sus componentes segmentarios y desplazamiento hacia abajo o hacia la izquierda de un conducto sectorial. Las variaciones anatómicas se detectan mediante el cartograma intrahepático durante la colangiografía peroperatoria. Es indispensable saber reconocer y enumerar los diferentes conductos sectoriales para poder garantizar que no falte ninguno. Las variaciones «con riesgo» son aquellas que modifican la anatomía del pedículo. La confluencia de un conducto cístico corto puede realizarse con uno de los conductos hepáticos derechos subdivididos.
Antecedentes de cirugía abdominal
Un antecedente de cirugía abdominal justifica la creación de un neumoperitoneo mediante la técnica «abierta» debido a que resulta imposible prever con seguridad que no exista ninguna adherencia visceral a la pared abdominal. Sólo un cirujano experimentado en laparoscopia puede considerarse autorizado a realizar una colecistectomía laparoscópica en caso de que existan antecedentes de cirugía supra-mesocólica.
Después de crear el neumoperitoneo, se deben elegir zonas libres de adherencias para introducir, poco a poco, los demás trocares necesarios para la intervención y crear mediante disección un espacio infrahepático útil para la colecistectomía.
Obesidad
La obesidad conlleva más dificultades operatorias en el hombre que en la mujer. La creación del neumoperitoneo es delicada, sea cual sea la técnica elegida, debido al espesor de la pared. El peso del panículo adiposo abdominal justifica el aumento de la presión intraabdominal a 15 mm Hg. La posición proclive utiliza la gravedad para hacer descender la cubierta epiploica y mejora las condiciones de ventilación peroperatoria al disminuir la presión de las vísceras sobre las cúpulas diafragmáticas. Frente a las dificultades reales de esta cirugía en el paciente obeso, se deben valorar todos los beneficios que pueden obtenerse de una intervención que intenta minimizar la morbilidad parietal, más frecuente en estos pacientes.
Embarazo
Durante el embarazo pueden realizarse procedimientos de cirugía laparoscópica. De forma esquemática, una operación quirúrgica durante el primer trimestre del embarazo corre el peligro de desencadenar un aborto, y durante el tercer trimestre, un parto prematuro. Por tanto, el trimestre
«Óptimo» para esta operación, cuando es absolutamente necesaria, es el segundo. La indicación de colecistectomía en el embarazo se reserva a las pacientes que tienen signos clínicos, analíticos y ecográficos (microlitiasis) que indican una posible migración de los cálculos al colédoco. Durante el segundo trimestre de embarazo también se puede realizar una colangiografía peroperatoria.
Desde el punto de vista técnico, se recomienda utilizar una técnica abierta para crear el neumoperitoneo y evitar el ombligo para el primer trocar. La localización de los trocares se desplaza más hacia el hipocondrio derecho a medida que avanza la edad gestacional. La presión intraabdominal está limitada a 10 mm Hg, o incluso a 8 mm Hg.
Conversión a laparotomía en los casos difíciles
La transformación peroperatoria de una intervención por vía laparoscópica en laparotomía se produce en el 1-3% de las patologías litiásicas vesiculares no complicadas y en el 10-30% de las formas complicadas [15]. He aquí las principales indicaciones:
- Todas las situaciones difíciles de disección quirúrgica (colecistitis aguda, colecistitis escleroatrófica, fístula biliodigestiva, síndrome de Mirizzi. etc.) cuando la experiencia del cirujano es limitada.
- Todos los procesos inflamatorios locales en los que la disección se considera peligrosa en la región del pedículo hepático, en particular si no hay un reconocimiento anatómico claro tras una duración significativa de la disección.
- En caso de complicación peroperatoria: hemorragia, fuga biliar de origen desconocido en ausencia de perforación vesicular, lesión biliar claramente documentada, lesión vascular o visceral. imposibilidad de recuperar totalmente cálculos diseminados dentro de la cavidad peritoneal.
- En caso de duda en cuanto a la integridad del árbol biliar en la epo (ausencia de opacación de las vías biliares altas, árbol biliar hepático derecho incompleto, extravasación del agente de contraste).
La conversión es una prueba de seguridad quirúrgica y debe ser percibida como tal por el cirujano. Siempre es mejor una conversión «con éxito» que una colecistectomía laparoscópica con complicaciones biliares, digestivas y hemorrágicas graves.
¿Cuándo debe efectuarse la conversión en laparotomía?
•Disección difícil (colecistitis, etc.) cirujano poco experimentado.
•Ausencia de reconocimiento anatómico claro.
•Complicación peroperatoria: hemorragia, fuga biliar complicada, lesión vascular o visceral, etc.
•Duda en cuanto a la integridad del árbol biliar (epO).
Complicaciones postoperatorias
Traumatismo quirúrgico de la VBP
Se trata del accidente peroperatorio más grave de la colecistectomía laparoscópica, a menudo con complicaciones graves para el paciente y problemas médico-legales para el cirujano.
Hemorragia
Las complicaciones hemorrágicas pueden producirse en varias circunstancias. Hemorragia difusa en caso de colecistitis aguda
En general, fuera de las alteraciones de la coagulación, la 22 «barohemostasia» asociada con el neumoperitoneo es suficiente para controlar las hemorragias difusas en sábana. No obstante, la presencia de sangre nubla la imagen; por una parte, es preciso disponer de una cámara endoscópica y, por la otra, irrigar con frecuencia el campo quirúrgico con suero fisiológico. Es preciso evitar emplear electrocoagulación en exceso.
¿Qué hacer en caso de hemorragia aguda?
•Pinzamiento en bloque o compresión del foco hemorrágico.
•Trocar y elementos auxiliares adicionales.
•Lavado-aspiración.
•Disección e identificación de la estructura vascular lesionada.
•Hemostasia por un clip electivo o con la pinza bipolar.
•Conversión y reparación con hilo fino si está lesionada la arteria hepática o su rama derecha.
Hemorragia aguda
La hemorragia puede producirse a partir de la arteria cística, de la rama derecha de la arteria hepática o más raramente de la vena porta. Con frecuencia, el sangrado es espectacular y, por una parte, conviene no ser presa de pánico y, por otra, hacer retroceder la óptica a distancia del jet (chorro) arterial para evitar mancharse y, perder así, la visión del campo operatorio, especialmente útil en esta situación de emergencia. El gesto de hemostasia comprende las etapas siguientes:
- En primer lugar, un gesto de hemostasia transitoria que contempla pinzar en bloque la arteria lesionada con una pinza fenestrada atraumática o comprimirla por medio de la cánula de aspiración. En ningún caso se emplearán la electrocoagulación o la colocación de un clip a ciegas.
- Si es preciso (p. ej., en un paciente obeso) debe añadirse de nuevo un trocar suplementario y/o llamar a un cirujano experimentado.
- No debe aspirarse de manera permanente, lo cual suprime el neumoperitoneo y, por consiguiente, la visión del campo operatorio.
- Lavar el foco hemorrágico y aspirar por contado.
- Disección de la estructura arterial en cuestión.
- Realizar la hemostasia definitiva por medio de un clip colocado electivamente o aplicando la pinza bipolar sobre el foco de hemorragia.
- En caso de lesión de la rama derecha de la arteria hepática, especialmente expuesta en caso de una arteria cística corta, no debe pinzarse el vaso, sino efectuar una conversión a laparotomía a fin de reparar escrupulosamente la arteria con hilo monofilamento 5 o 6/0.
Durante el tiempo de conversión requerido se detiene la hemorragia mediante una pinza fenestrada atraumática situada lo más próxima posible sobre el foco hemorrágico.
Lesión hepática durante la disección del lecho vascular
Se produce cuando hay un error en el plano de despegamiento ente el hígado y la VB, lo cual sucede en determinadas colecistitis. El plano de disección es a veces difícil de encontrar, o es inexistente, y si se desea resecar por completo la VB se sitúa inevitablemente en el seno del parénquima hepático, de ahí el riesgo de hemorragia y/o de fístula biliar.
En caso de sangrado demasiado abundante es preferible mantener una parte de la pared vesicular en contacto con el hígado. En general, la hemorragia se controla fácilmente a través de uno de los medios siguientes: eledrocoagulación mono o bipolar, vaporización con argón, colocación de compresas hemostásicas reabsorbibles, compresión simple con un instrumento atraumático o mediante una gasa o puntos de sutura en X.
Hemorragia en el orificio de trocar
Por regla general todos los trocares deben retirarse uno a uno bajo control endoscópico. El hecho de no detectar una hemorragia arterial en el orificio de trocar expone a un riesgo de hemoperitoneo postoperatorio. Un sangrado moderado puede controlarse fácilmente a través de diferentes medios: compresión interna con la ayuda del trocar propiamente dicho o de un instrumento, eledrocoagulación desde el interior, una sonda de Foley introducida a través del orificio del trocar, retirada de un balón hinchado, y manteniendo la tracción con una pinza de Kocher colocada a ras de piel durante 5 mino En caso de hemorragia significativa o, en caso de sangrado arterial (arteria epigástrica), será preciso recurrir a puntos totales transparietales o a agrandar la incisión y llevar a cabo una hemostasia electiva (puntos en X).
Lesión digestiva
Las lesiones digestivas (gástrica, duodenal, cólica, etc.) en el curso de una colecistectomía laparoscópica son muy infrecuentes pero pueden producirse ya sea en la introducción a ciegas de la aguja de Veress o del primer trocar, o en el momento de resecar adherencias inflamatorias perivesiculares.
Más que su prevención mediante una técnica adecuada (p. ej., sonda gástrica previa a la introducción de la aguja de Veress para prevenir una lesión gástrica), es sobre todo la necesidad absoluta de su detección peroperatoria lo que importa con el fin de evitar una peritonitis postoperatoria no detectada. Hay que controlar las lesiones viscerales perforantes con una brecha posterior que puede pasar desapercibida. La reparación mediante sutura puede efectuarse por vía laparoscópica si la exploración de la lesión es completa y la experiencia quirúrgica en suturas intraperitoneales es adecuada.
Abertura accidental de la VB y diseminación Iitiásica intraperitoneal
Esta complicación, que se produce a menudo durante la disección de una colecistitis difícil no es tan banal como podría pensarse, ya que puede ser responsable de un absceso postoperatorio tardío y recidivante sobre una litiasis intraperitoneal residual. En este contexto clínico, una radiografía de abdomen sin preparación o un examen tomodensitométrico sin inyección del abdomen pueden poner de manifiesto cálculos residuales, que a veces van a justificar una re intervención quirúrgica.
En la práctica, desde el momento que tiene lugar una perforación vesicular se aconseja extraer los cálculos uno a uno con la pinza o colocarlos en un saco de extracción, dispuesto en posición de espera en la cara superoexterna del hígado derecho. A veces, es posible volver a cerrar la perforación (sutura, endoloop, etc.). En caso de perforación vesicular deberá retirarse de la cavidad peritoneal la totalidad de los cálculos perdidos y extraerlos con la VB dentro de un saco de protección.
Lesiones biliares
La complicación más frecuente que se observa durante la colecistectomía laparoscópica es la rotura de la pared de la vesícula. La salida de bilis, incluso infectada, puede controlarse rápidamente mediante lavado-aspiración. Se aconseja entonces vaciar completamente el contenido biliar de la vesícula ya que es necesario recuperar todos los cálculos. Se han descrito varias complicaciones relacionadas con los cálculos abandonados en el abdomen o encontrados de forma secundaria en el trayecto de un trocar. El lavado y la aspiración son útiles para recuperar pequeños cálculos que se pegan a la cánula y pueden entorpecer el funcionamiento. Hay que buscar posibles cálculos bajo el hígado, en la punta del lóbulo derecho, en el espacio interhepatodiafragmático y por detrás del pedículo.
La complicación biliar más grave durante la colecistectomía laparoscópica es la lesión del conducto biliar. Este riesgo se ha multiplicado por tres en la técnica laparoscópica frente a la laparotomía: 0,6 frente a 0,2 %, respectivamente. Las estadísticas más recientes siguen hablando de lesión biliar en el 0,6 al 0,8 % de los casos. Este riesgo es más significativo durante las primeras 20 colecistectomías: se han descrito cifras que alcanzan el 2 %. No existe relación demostrada entre el riesgo de lesión biliar y las variaciones anatómicas del pedículo biliar. La mayoría de las lesiones biliares aparece durante colecistectomías que no presentan especial dificultad. Un estudio poblacional detectó una disminución del riesgo de lesión biliar durante la colecistectomía cuando ésta se acompañaba de una colangiografía peroperatoria. En todos los casos en los que la colangiografía detecte una lesión biliar, sólo debe continuar la laparoscopia un cirujano experimentado. Cualquier otro cirujano deberá convertir la cirugía en laparotomía y obtener mediante estudio radiológico y quirúrgico una valoración precisa de la complicación. En función de la habilidad del cirujano o del nivel técnico del centro, se decidirá entre una reparación inmediata o la derivación del paciente a un servicio especializado.
Complicaciones postoperatorias
El postoperatorio de una colecistectomía laparoscópica tiene que ser «simple». Cualquier signo anormal en las primeras 24 horas debe tenerse en cuenta: dolor, fiebre, íleo o imposibilidad para alimentarse.
Complicaciones biliares
La fuga de bilis es la complicación más temida. En alrededor del 15 % de los casos, se trata de un goteo biliar por el drenaje colocado al final de la intervención. En el resto de los casos, se trata de un derrame biliar generalizado intraperitoneal (coleperitoneo) o un «bilioma» infrahepático. La sensibilidad de los signos y síntomas del coleperitoneo postoperatorio es mala. En uno de cada dos casos se presentan dolor, sensación de malestar general, ictericia o un aumento de la bilirrubina. En tres o cuatro casos de cada diez se observa fiebre, meteorismo y náuseas o vómitos. Menos de un paciente de cada cinco presenta signos peritoneales. El hecho de que la fístula biliar se drene, disminuye la frecuencia del dolor, de la fiebre y del íleo reflejo, pero no reduce la frecuencia de ictericia y de signos peritoneales. En uno de cada cuatro casos, se observa un cuadro clínico que recuerda a una colangitis, se haya realizado drenaje o no. El diagnóstico de la acumulación intraperitoneal se realiza inicialmente mediante ecografía y se completa con una tomografía computadorizada abdominal. El diagnóstico de la fuga de bilis se confirma al observar la imagen en la colangiografía retrógrada, sobre todo, o en la colangiografía directa si se había colocado un drenaje biliar externo. La fistulografía del tubo de drenaje es inútil en el postoperatorio precoz. Las fístulas biliares que se originan en un conducto accesorio en el lecho vesicular pueden secarse de forma espontánea o justificar una nueva exploración mediante laparoscopia o laparotomía. Las fístulas biliares por relajación del muñón cístico se diagnostican mediante la introducción retrógrada endoscópica de contraste y se tratan mediante endoprótesis con o sin esfinterotomía. Las fístulas biliares por lesiones del colédoco tienen un tratamiento más complejo y no forman parte de este capítulo. Si no se trata de un centro especializado, deben ser drenadas y derivadas sin retraso para llevarlo a cabo.
Complicaciones hemorrágicas
La complicación hemorrágica más grave, y que puede ser rápidamente mortal, es la lesión de los vasos retroperitoneales durante la creación del neumoperitoneo, que puede pasar desapercibida durante la intervención. El diagnóstico se sospecha cuando aparece un shock en la sala de despertar. Se debe volver inmediatamente al quirófano y realizar una laparotomía de urgencia para evitar lo peor.
La hemorragia en uno de los orificios de los trocares es mucho menos alarmante, aunque pueda acabar de forma secundaria en una transfusión o incluso en una reintervención. El diagnóstico viene dado por la pérdida sanguínea postoperatoria cuya causa sólo se averigua cuando se vuelve a intervenir. La laparoscopia no es el método más «adecuado» para volver a explorar un hemoperitoneo. Es difícil realizar el lavado y la aspiración de los coágulos mediante laparoscopia y esta nueva exploración debe terminar con la certeza de haber identificado con precisión el origen de la hemorragia. Por tanto, se recomienda realizar una laparotomía si la primera reexploración laparoscópica no alcanza el objetivo previsto.
Cuidados postoperatorios
Habitualmente, las repercusiones postoperatorias de una colecistectomía laparoscópica son muy simples, incluso en caso de colecistitis aguda. La reanudación del tránsito intestinal y la rehabilitación funcional del paciente son rápidas, hasta el punto de que la gran mayoría de los pacientes abandonan el hospital entre el primero y el tercer día después de la intervención quirúrgica. Se considera que la persistencia de los dolores abdominales más allá de dos o tres días después de la cirugía, así como la presencia de bilis o de sangre en el drenaje infrahepático debe hacer pensar en la posibilidad de una complicación. Ello debe llevar a realizar un control biológico y una prueba de imagen, la mayoría de veces una ecografía. Se considera anodino observar una discreta alteración postoperatoria transitoria de la biología hepática, pero la aparición de una colestasis debe hacer pensar en una complicación biliar. Del mismo modo, en la ecografía es habitual la presencia de una colección a nivel del lecho vesicular, aunque el aumento de dicha colección o la presencia de una ascitis difusa deben hacer pensar de nuevo en una complicación biliar.
Bibliografía
& Ashcraft. Cirugia pediátrica. Mc Graw hill.
& Barkun, 1993. Randomised controlled trial of laparoscopic versus mini cholecystectomy. Barkun js, barkun an, sampalls js et al. Lancet 1993, 341: 1214-1215.
& Bingener, 2002. Reasons for conversion from laparoscopic to open cholecystectomy: a 10-year review. Bingener-casey j, richards ml, strodel we et al. J gastrointest surg 2002, 6: 800-805.
& Bismuth, 1981. Les traumatismes opératoires de la voie biliaire principa/e. Monographies de l'association fran~ aise de chirurgie. Bismuth h, lazorthes f. Masson, paris, 1981, vol 1.
& Blumgart Cirugía de hígado, páncreas, y vía biliar. 5th Edición. Editorial Saunders
& Bockus. Gastroenterología. Salvat.
& Brunicardi. Schwartz, Principios de cirugía. 9na. Edición. Mc Graw Hill.
& Carico. Atlas tratamiento quirúrgico del trauma. Mc Graw Hill.
& Champault, 1996. Serious trocar accidents in laparoscopic surgery: a french survey of 103852 operations.Champault g, cazacu f, taffinder n. Surg laparosc endosc 1996, 6: 367-370.
& CMCG. Tratado de cirugía general. 2da. edición. Manual moderno
& Cunningham. Williams obstetricia. Panamericana.
& Díaz rubio. Trastornos motores del aparato digestivo. Panamericana.
& Drossman. The functional Gastrointestinal Disorders, Rome III.
& Elsevier 2014. Tratado de Cirugía del aparato digestivo.
& Elsevier 2014. Tratado de Cirugía plástica.
& Elsevier 2014. Tratado de Cirugía General.
& Elsevier 2014. Tratado de Ginecología y obstetricia.
& Elsevier 2014. Tratado de Medicina.
& Elsevier 2014. Tratado de Pediatría.
& Elsevier tratado de Urología, 2014.
& Flum, 2003. Intraoperative cholangiography and risks of common bile duct injury during cholecystectomy. Flum d, delllnger e, cheadle a et al. Jama 2003, 289: 1639-1644.
& Garber, 1997. Early laparoscopic cholecystectomy for acute cholecystitis. Garber sm, korman j, cosgrove jm, cohen jr. Surg endosc 1997, 11: 347-350.
& Gigot, 1997. The dramatic reality of biliary tract injury during laparoscopic cholecystectomy: an anonymous multicentric belgian survey of 65 patients. Gigot jf, etienne j, aerts r et al. Surg endosc 1997,11: 1171-1178.
& Gleicher. Tratamiento de las complicaciones clínicas del embarazo. Panamericana
& Gliedman. Atlas de técnicas quirúrgicas. Mc Graw Hill.
& Goldberg. Fundamentos de cirugía anorectal. Noriega Limosa.
& Gutiérrez Samperio. Fisiopatología quirúrgica del aparato digestivo. 2da. edición. Manual Moderno.
& Hinman. Atlas de cirugía urológica. Mc Graw Hill.
& Kiviluoto, 1998. Randomised trial of laparoscopic versus open cholecystectomy for acute and gangrenous cholecystitis.Kiviluoto t, siren j, luukkonen p, kivilaakso e. Lancet 1998, 351: 321-325.
& Madden. Atlas de técnicas en cirugía.
& Madrazo, Nutrición y gastroenterología pediátrica. Mc Graw Hill.
& Maingot-Zinner. Operaciones abdominales. 11 va. edición Panamericana.
& Majeed, 1996. Randomised, prospective, single-blind comparison of laparoscopic versus smallincision cholecystectomy. Majeed aw, troy g, nicholl jp et al. Lancet 1996, 347: 989-994.
& Mattox. Trauma. Mc Graw hill.
& Mayagoitia. Hernias de la pared abdominal. 2da. edición. Mc Graw Hill.
& Mcmahon, 1994. Laparoscopic versus minilaparotomy cholecystectomy: a randomised trial. Mcmahon aj, russel it, baxter jn et al. Lancet 1994, 343: 135-138.
& Michael Henry. Cirugia clínica. Masson.
& Misiewicz. Atlas de gastroenterología clinica. Mossby.
& Mouiel, 1991. La cholécystectomie par laser en c~liochirurgie. Testas p., delaitre b. Chirurgie digestive par voie ca2lioscopique. Mouiel j, katkhouda n. Maloine, paris, 1991 : 113-119.
& Navez, 2001. Safety of laparoscopic approach for acute cholecystitis: retrospective study of 609 cases.Navez b, mutter d, russier yet al. Worldj surg 2001,25: 1352-1356.
& Neudecker, 2002. The e.a.e.s. clinical guidelines on the pneumoperitoneum for laparoscopic surgery. Neudecker j, sauerland s, neugebauer eet al. Surg endosc 2002, 16: 1121-1143.
& Neugebauer, 2000. Recommendations for evidence-based endoscopic surgery. The updated eaes consensus deve/opment conferences. Neugebauer e, sauerland s, troidl h. Springer-verlag, 2000.
& Nyhus. Dolor abdominal. Editorial paramericana
& O´Neil. Pediatric surgery. Mosby.
& Perera. Cirugía de urgencia. 2da. edición. Interamericana.
& Pérez de Gallo, Dietas. Ediciones científicas la prensa medica mexicana.
& Quintero. Infeccion en cirugía. Editoral panamericana
& Robles. Nutrición en el paciente críticamente enfermo. Mc Graw Hill.
& Rock. Te Linde. Ginecologia quirúrgica. Panamericana
& Sabiston. Atlas de cirugía. Mc Graw Hill.
& Sabiston. Tratado de cirugía. Mac Graw Hill
& Skandalakis. Hernias. Mc Graw Hill.
& Skandalakys. Complicaciones anatómicas en cirugía general. Mc Graw Hill.
& Stoopen. Radiologia e imagen diagnóstica y terapéutica. Abdomen Tomo I. Editorial Lippincott.
& Suros. Semiologia médica y técnica exploratoria. Masson.
& Testut-Latarget. Anatomía Humana. Salvat.
& Valenzuela. Gastroenterología y hepatología. Mediterráneo
& Villazón- arenas. Nutrición enteral y parenteral. Interamericana
& Way. Diagnóstico y tratamiento quirúrgicos. Manual moderno.
& Wolfe. Terapeutica de los trastornos digestivos. Mc Graw Hill.
& Yoshida, 1996. Practical c1assification of the branching types of the biliary tree: an analysis of 1,094 consecutive direet cholangiograms Yoshida j, chijilwa k, yamaguchi k et al.. J am col/ surg 1996, 182: 37-40.
& Zuidema-Shackelford. Cirugía del aparato digestivo. 6ta edición. Interamericana.


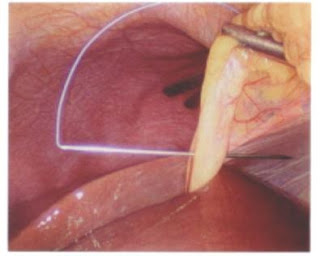




































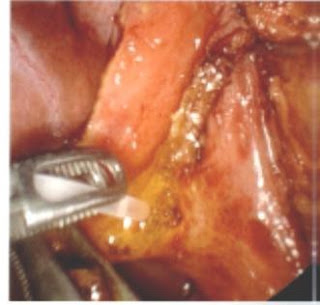


No hay comentarios.:
Publicar un comentario